東京工業大学(東工大)、京都大学(京大)、東北大学、理化学研究所(理研)の4者は6月7日、がんのバイオマーカーである特定の「マイクロRNA」(miRNA)を選択的に認識し、「AND演算」の結果を出力できる「RNA液滴コンピュータ」の開発に成功したと共同で発表した。
同成果は、東工大 情報理工学院 情報工学系の瀧ノ上正浩教授、同・鵜殿寛岳博士研究員(学術振興会特別研究員)、同・范敏之大学院生(研究当時)、同・齊藤洋子技術員(研究当時)、京大 iPS細胞研究所 未来生命科学開拓部門の齊藤博英教授、同・大野博久助教、東北大大学院 工学研究科 ロボティクス専攻の野村M.慎一郎准教授、理研 生命機能科学研究センターの清水義宏チームリーダーらの共同研究チームによるもの。詳細は、米国化学会が刊行するナノサイエンス/テクノロジーに関する全般を扱う学術誌「ACSNano」に掲載された。
DNAやRNAからなる直径数nmのナノ構造体(モチーフ)は、自発的に集合し高い流動性を持つ直径数μmの液滴(マイクロ構造体)を形成することが可能だ。モチーフはXやYなどのような形状で分岐構造を持ち、末端同士で相互作用する。また、塩基対形成ルールに従ってモチーフ同士の相互作用を自在にプログラムでき、それにより液滴同士を自在に融合・分離させることも可能だ。
近年、DNAでのAND演算を実行する液滴が報告されていたが、一方のRNAは機能性を持たない液滴の形成が報告されているのみだった。RNAはDNAと比べると機能も構造もはるかに多様で、DNAよりも複雑な相互作用をすることから、それらを活かした多様な機能・構造を発現するRNA液滴の実現は、プログラマブルで高機能な液-液相分離液滴の発展に不可欠な一歩だという。そこで研究チームは今回、「特定のmiRNAが2種類入力された時だけRNA液滴が溶解する」という挙動の実現を目指したとする。
モチーフ間の相互作用としては、遺伝子発現制御などに関わる、末端にヘアピン状のループ構造を持つRNA同士が結合する「キッシング・ループ(KL)相互作用」がRNA液滴の形成原理とされた。
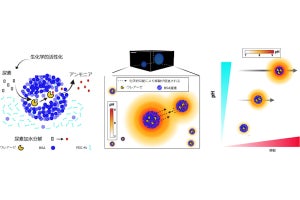
AND演算RNAモチーフは、KLを含むXs1~Xs4の配列の他に、サイドに2つの突起構造STH1とSTH2を持つ。先端に2種類のmiRNA(“m1”と“m2”)の同色部分と結合する配列がある。たとえばm1が入力された場合、赤の部分はSTH1の赤色の配列と結合する。これを足がかりとして、m1の緑の部分はSTH1の緑の配列と結合し、もともとSTH1と結合していたXs4の緑の配列は切り離される。この鎖置換反応がSTH2でも起こる結果、モチーフは2つに分離する。初期構造はネットワーク状の構造だが、分離後は鎖状の構造へと変化する。初期構造は水に溶けにくく液滴として存在可能だが、鎖状構造は水に溶けやすいため、m1およびm2が入力された時だけ液滴は溶解する仕組みだ。
-
入力されたmiRNAに対してAND演算を実行するRNA液滴。(a)入力の1と0はそれぞれのmiRNAが「ある」時と「ない」時を意味する。miRNA-1、miRNA-2の両方とも「ある」時(1と1の時)だけ出力が1になる。その時だけモチーフは2つに分裂し、液滴が溶解する挙動として現れる。(b)モチーフの分離メカニズムの模式図。(c)モチーフの結合の様子(出所:共同プレスリリースPDF)
実際にAND演算RNAモチーフから液滴が作製され、miRNAの入力に対する演算例として、乳がんのバイオマーカーである4種類のmiRNA(m1~m4)が用いられた。まず、m1およびm2に対するAND演算が実行された結果、顕微鏡観察により、AND演算RNAモチーフがRNA液滴を形成することが確認された。
次に、各入力の組み合わせの結果生じるRNA液滴の様子が観察された。すると、入力[1,1]の時は25分ほどで大半の液滴は溶け、最終的に見えなくなった一方で、それ以外の入力では、3時間半以上の観察を通じて液滴は溶解しなかったとする。これにより、RNAに特有の相互作用でも液滴を形成できるという今回の研究目的が達成された。
-
RNA液滴によるAND演算の実行。(a)乳がんのバイオマーカーである4つのmiRNA。m1とm2が今回のAND演算でターゲットとされた配列(m3と4は非ターゲット配列)。(b)入力の各組み合わせおよび対応するモチーフの最終構造。入力[1,1]の時だけモチーフが2つに分離。(c)モチーフの結合態様。入力[1,1]以外はすべてネットワーク状構造が保存される。(d)各入力に応じたRNA液滴の変化。入力[1,1]の時だけ液滴が溶解する。スケールバーは50μm(出所:共同プレスリリースPDF)
最後に、幅広い応用を可能にするため、RNA液滴の演算結果をもっと簡便かつ安価に検出する手法として、RNAとDNAをそれぞれ異なる色で染められる、安価な細胞染色液「メチルグリーン・ピロニン」を用いた手法も開発された。m1とm2の両方が加えられた場合は、RNA液滴が溶解するために染色は目視できず、それ以外の入力の場合は染色されたRNAの沈殿物が直接目視された。RNA液滴によるAND演算の出力結果を、高価な機器や試薬なしで検出することに成功したのである。
-
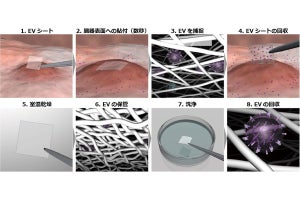
直接目視によるAND演算の検出。(a)チューブ内にあるRNA液滴にmiRNAもしくはバッファーを入力後、メチルグリーン・ピロニン染色液を加えた後の様子。m1もm2も入力なし(A・E)。両方とも入力あり(B)。片方だけ入力あり(C・D)。(b)チューブ底の近接撮影。出力が1の時は液滴が溶解するため、染色液では染まらない。一方、出力が0の時は液滴が保存されているため、染色液でマゼンタ色に染まったRNAが目視できる。スケールバーは(a)5mm、(b)2mm(出所:共同プレスリリースPDF)
今回の研究成果は、がんの早期診断技術への活用に加え、結果を目視可能なことから僻地や発展途上国などでの病気、ウィルス感染診断の拡充にもつながるという。また、複数の論理演算を組み合わせたより高度な論理回路を組み込んだRNA液滴コンピュータへの展開も可能とする。さらに、液滴を構成するモチーフの配列をコードしたDNAを鋳型として細胞に注入して、細胞の転写機構を利用してRNA液滴を発現する将来的な技術への重要な足がかりも得られたとしている。