名古屋大学(名大)と科学技術振興機構(JST)は2月2日、発がんヘルペスウイルス「Epstein-Barr(EB)ウイルス」が免疫細胞の一種である「B細胞」を不死化する際にウイルス因子「BNRF1」が宿主因子「IFI27」を誘導し、安定した細胞増殖能を獲得することを明らかにしたと発表した。
同成果は、名大大学院 医学系研究科 ウイルス学の木村宏教授、同・佐藤好隆准教授、同科 血液・腫瘍内科学の清井仁教授、同・佐合健大学院生、同科 生体反応病理学の豊國伸哉教授、名古屋市立大学 ウイルス学の奥野友介教授、藤田医科大学ウイルス学の村田貴之教授らの共同研究チームによるもの。詳細は、病原体生物学または病原体と宿主の相互作用に関する全般を扱う学術誌「PLOS Pathogens」に掲載された。
ヘルペスウイルス科のDNAウイルスであるEBウイルスは、成人の90%以上に感染していると見積もられているが、その大半は症状を示さず、体内で主にB細胞に潜伏して過ごすとされている。ただし、まれに「びまん性大細胞型B細胞リンパ腫」や「バーキットリンパ腫」、「移植後リンパ増殖症」などの血液がんである「リンパ腫」の原因となることも分かっている。
ウイルスは、ヒトなどの宿主の細胞に侵入し、自らの遺伝子を巧みに活用して宿主細胞本来のDNAを改変して乗っ取り、自己に都合のよい“ウイルス生産工場”などに宿主細胞を作り替えてしまう。EBウイルスの遺伝子は多くて70以上あり、多くの遺伝子においてその機能はまだ完全には理解されていない。
びまん性大細胞型B細胞リンパ腫は、悪性リンパ腫の中で最も患者数が多く、全リンパ腫のおよそ30~40%を占めるとされている。同リンパ腫においては、腫瘍細胞内にEBウイルスが存在する症例とEBウイルスが存在しない症例では、EBウイルスが存在する症例の方が、予後が悪いことが知られており、一般にEBウイルス関連リンパ腫は抗がん剤が効きにくいとされている。そのため、EBウイルス関連リンパ腫に対する新たな治療法の開発が求められていた。
ヒトのヘルペスウイルスには、腫瘍の原因になるものとならないものが存在する。両者は多くの遺伝子を共有しているが、今回の研究では腫瘍を起こすヘルペスウイルスにのみ存在する遺伝子BNRF1が着目され、同遺伝子が腫瘍細胞に与える影響について解析を試みることにしたという。
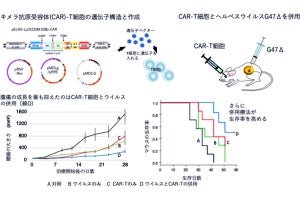
BNRF1を欠損させた組み換えEBウイルス「EBV/BNRF1-KO」(KOウイルス)を作成し、B細胞への感染を行ったところ、KOウイルスはB細胞を不死化させたが、その活性は野生型(遺伝子を欠損させていない親株)に比べて低く、感染細胞の増殖能も低下していることが判明。このKOウイルス感染細胞を免疫不全マウスに移植したところ、マウスの体内で腫瘍を形成することができず、BNRF1遺伝子の欠損によりEBウイルスの病原性が低下することが確認されたという。
遺伝子発現解析が行われたところ、BNRF1遺伝子の発現で影響を受ける宿主遺伝子が、ミトコンドリアに局在するタンパク質の遺伝子である「IFI27」であることが同定された。また、EBウイルス感染細胞においてIFI27の発現の低下が行われたところ、BNRF1を欠損させた時と同じ表現型を示すことが示されたとするほか、BNRF1の欠損やIFI27の発現低下によって、EBウイルス感染細胞内では活性酸素が蓄積し、そのためエネルギー産生が十分に行えず、細胞内ATP量が減少することが確かめられたという。これはEBウイルスのBNRF1と宿主因子IFI27は、感染細胞内で活性酸素の発生を抑制し、ウイルス感染細胞の安定的な増殖に寄与していることを示す結果だという。
EBウイルス感染細胞はヒトの身体の中に潜み、いずれは腫瘍細胞へと変化すると考えられている。今回の研究で、EBウイルス感染細胞の安定的な細胞増殖にウイルス因子のBNRF1と宿主因子のIFI27が関与していること、および、BNRF1やIFI27を阻害するとEBウイルス感染細胞の病原性が低下することが示されることとなったが、研究チームではBNRF1とIFI27は、共に感染細胞でのエネルギー産生に関与しているため、今回の研究成果により、ウイルスによるエネルギー産生が新たな治療標的となる可能性が示唆されたとしている。