奈良先端科学技術大学院大学(NAIST)は1月4日、多能性幹細胞を注入して目的の臓器を作製する「胚盤胞補完法」を応用し、肺欠損マウスの体内に、異種であるラットの多能性幹細胞由来の肺を作り出すことに成功したと発表した。
同成果は、NAIST 先端科学技術研究科 バイオサイエンス領域 器官発生工学研究室の由利俊祐助教、同・村瀬勇気大学院生(研究当時)、同・磯谷綾子准教授の研究チームによるもの。詳細は、発生生物学に関する全般を扱う学術誌「Development」に掲載された。
肺でガス交換を担う肺胞は慢性的な損傷からは回復できないため、慢性閉塞性肺疾患(COPD)などの肺疾患は治癒が難しく、全世界で3番目に多い死因となっている。COPDなどの抜本的な治療法は現時点で肺移植しかなく、ドナー不足という深刻な問題を抱えている。現在、多能性幹細胞から生体外で肺を作製することが世界的に試みられているが、複雑な構造の肺を立体的かつ機能を有する状態で作製するまでには至っていないという。
そこで注目されているのが、動物の持つ発生システムを利用した胚盤胞補完法を用いた臓器作製だ。同手法は、臓器欠損モデル動物の初期胚(胚盤胞)に野生型の多能性幹細胞を注入したキメラ動物の体内で、多能性幹細胞由来の臓器を作るものである。
これまで胚盤胞補完法を用いたマウスとラットの異種間キメラ動物(以下、MRキメラ)の体内において、膵臓や胸腺、腎臓などは作製されていたとのこと。しかし、肺に関する報告はなかったとする。そこで研究チームは今回、同手法を用いてラット多能性幹細胞由来の肺をMRキメラの体内で作製可能かどうかを確かめたという。
一般的な胚盤胞補完法では、遺伝子欠損の臓器欠損モデル動物が用いられている。しかし肺欠損は致死的なため、その初期胚はほかと比べて4分の1しか得られず、実験効率が悪かったとする。さらに、臓器欠損の表現型を持つ遺伝型の細胞でも、正常細胞が混在するキメラになると、正常細胞の影響で、遺伝子欠損の表現型がレスキューされ、遺伝子欠損細胞も欠損する臓器に寄与する可能性も考えられたという。
今回の研究ではそれらの課題を解決するため、肺の発生に重要な遺伝子(Fgfr2b遺伝子)を欠損したES細胞を作製し、胚盤胞補完法とは逆に、野生型の胚盤胞へそのES細胞を注入する「逆・胚盤胞補完法」という手法が採用された。同手法では、すべてのMRキメラが肺欠損細胞と正常細胞を有するため、実験効率が向上するとともに、赤色蛍光タンパク質で標識した肺欠損ES細胞を用いることで、肺欠損細胞の分布を追跡も可能である。
そして実験の結果、MRキメラに10%以上の割合で正常細胞が含まれると、肺が確認されることが突き止められ、Fgfr2b遺伝子欠損動物の体内に肺を作り出すための条件であることが判明。また、ガス交換を行う肺の上皮組織には同遺伝子の欠損細胞が確認されなかったことから、同遺伝子欠損モデルでは、肺の上皮組織を野生型の細胞が補完していることが明らかにされた。
-
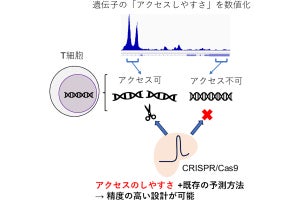
Fgfr2b-KOマウスを用いた解析。Fgfr2b-KO細胞は、肺の上皮(E-Cad+)細胞へ寄与していないことから、Fgfr2b-KOモデルを用いた場合、そのキメラ動物の肺上皮細胞は、野生型の細胞から構成されていることがわかった(出所:NAISTプレスリリースPDF)
次に、ラットES細胞をマウス初期胚へ注入した際に、ラット細胞がどの程度マウスの肺へ寄与できるのかが調べられた。すると、ラット細胞はほかの臓器と比較して、マウスの肺組織に寄与しやすく、MRキメラの個体の肺にラットの細胞が10%以上寄与できることが確認された。それにより、肺を持たないマウス細胞を用いれば、MRキメラ体内でラット多能性幹細胞に由来する肺を作り出せる可能性が高いことがわかったのである。
そこで研究チームは、完全にES細胞に由来する個体を作製する「四倍体胚補完法」を用いて、Fgfr2b遺伝子を欠損するマウスES細胞とラットES細胞に由来するMRキメラを作製し解析を実施。その結果、MRキメラの体内で、ラット多能性幹細胞に由来する肺を作り出せたことが確認されたといい、またその肺の上皮細胞の大半はラット細胞に置換されていたとした。
-
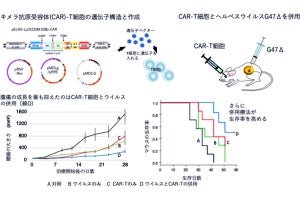
肺欠損マウス体内でのラット多能性幹細胞由来の肺の作製。(上)肺欠損するマウス初期胚に対し、ラット多能性幹細胞(緑色)が注入されたところ、ラット由来の肺(緑色)が作製された。(下)作製された肺の大部分は、ラット細胞(緑色)によって構成されていた。特に、上皮(E-Cad+)細胞はラット細胞のみで構成されていた(出所:NAISTプレスリリースPDF)
-
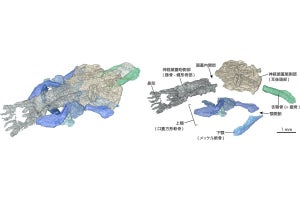
マウス体内で作製されたラット多能性幹細胞由来の肺の解析。(上)マウス体内で作製されたラット肺は、マウスの肺と比較して、肺胞内の空隙が狭かった。(下)マウス体内で作製されたラット肺は、未成熟マーカーであるSox9が発現しており、成熟していないことが示された(出所:NAISTプレスリリースPDF)
しかし、ラット由来の肺を持つMRキメラは呼吸しないため、生後15分以内に致死となることも判明。ラット肺を詳しく調べたところ、肺胞腔内に空隙が少なく、肺が未成熟状態である可能性が示された。ラットはマウスより2日遅く発生することから、肺の成熟状態を調べたところ、機能を持つ肺胞へと最終分化しておらず、それが原因で今回のラット肺は機能しなかったことが考えられたと結論付けている。
今回、胚盤胞補完法によりキメラ動物体内で機能を持つ肺を作製するためには、動物が固有に持つ発生の時間スケールを考慮する必要性もあることが示された。研究チームはこの成果について、将来的に、胚盤胞補完法を用いて動物の体内で肺を作製する可能性を示すものであり、再生臓器の移植医療の発展に貢献するものと期待されるとしている。