北海道大学(北大)と神戸大学の両者は10月25日、リチウムイオン電池(LIB)の正極活物質として広く使用されている「コバルト酸リチウム」(LiCoO2)を、低温かつ短時間で合成する手法の開発に成功したと共同で発表した。
同成果は、北大大学院 理学研究院の松井雅樹教授、神戸大大学院 工学研究科の水畑穣教授らの共同研究チームによるもの。詳細は、無機化学に関連する全般を扱う学術誌「Inorganic Chemistry」に掲載された。
正極活物質とは、蓄電池の正(プラス)極で起こる酸化還元反応を担う物質のことで、LIBの製造においては最もコストの高い部材であり、原材料価格だけに留まらず、その生産プロセスによるコストも課題となっている。LIBの正極活物質として広く利用されているのがLiCoO2で、800℃~1000℃という高温で10時間~20時間ほどの焼成工程を経て製造されているため、コストに加えて製造時の二酸化炭素(CO2)排出量の多さも大きな課題となっている。
そこでこれまで、LiCoO2を低温で合成する試みが検討されてきたが、500℃以下の温度では、LiCoO2とは結晶構造の異なるスピネル型(=低温相)LiCoO2が生成されることが報告されていた。そのため、求められている「層状LiCoO2」は高温のみで得られる高温相であると考えられてきたという。
そうした中、研究チームが一般的なセラミックスの合成法である固相法に代わるものとして開発したのが、「ハイドロフラックス法」だ。同手法は、出発原料の水酸化リチウムをやや過剰に使用し、そこに水酸化ナトリウムと少量の水を加えて、水酸化リチウムの融点を下げて反応温度で液相を形成することで、水酸化コバルトとの反応性向上を狙ったものだ。この反応は、300℃という低温でLiCoO2の結晶成長が促進されると同時に、不純物の生成を抑制できることがわかっていた。そこで今回の研究では、ハイドロフラックス法における反応過程での生成物の構造変化を詳細に追跡し、反応経路の解明を試みたという。
-
ハイドロフラックス法で合成されたLiCoO2の粉末X線回折図形(a)、電子顕微鏡像(b)。従来法を用いて300℃で合成した場合と比較して、シャープな回折ピークが結晶成長を示しており、電子顕微鏡像で確認できる粒子成長の様子とよく一致するという(出所:北大プレスリリースPDF)
そして詳細な追跡の結果、コバルト源の水酸化コバルトが岩塩型酸化コバルトへと構造変化し、それを経由して液相中に溶解し、液相中でリチウムと反応することでLiCoO2が形成されることが確認された。さらに、この反応過程の追跡で、LiCoO2の結晶成長が300℃到達後30分という短時間で完了することも明らかになったとする。この速い結晶成長について研究チームは、液相中で反応が進行することによるものと考えられるとしている。
-
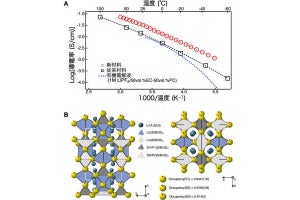
ハイドロフラックス法で合成されたLiCoO2と、固相法を用いて300℃で合成したLiCoO2の充放電曲線の比較。ハイドロフラックス法で合成された試料は、高い可逆容量が得られる(出所:北大プレスリリースPDF)
-
ハイドロフラックス法によって合成中の試料の構造変化を示すX線回折図形。300℃到達から15分程度で層状コバルト酸リチウムが生成され、30分で結晶成長が完了することが確認できた(出所:北大プレスリリースPDF)
また今回の研究では、ハイドロフラックス法を用いて、さらに低温の150℃でも層状LiCoO2が生成されることが確認されたとのことで、上述したようにこれまで層状LiCoO2は高温相であると認識されてきたのは間違いであり、広い温度域で安定相として得られることが実験的に証明された。
今回開発されたハイドロフラックス法と従来の固相法との違いは、基本的には出発原料の選択と組み合わせだけであり、特別な設備が必要ない点もハイドロフラックス法のメリットとなっている。このことから研究チームは、今回の手法が蓄電池材料合成プロセスの大幅な省エネルギー化、低コスト化およびCO2排出量の低減を実現可能な技術であると考えているとする。
また、今回の手法の適用範囲は蓄電池材料だけに限ったものではないといい、今後の開発を通じて、さまざまなセラミックス粉末製造への応用展開も期待されるとしている。