京都大学(京大)は10月6日、iPS細胞から成熟した「人工心筋組織」(ECT)の作製方法を開発し、これまで正確な疾患モデルのなかったところ、より正確な心筋症を再現することに成功したと発表した。
同成果は、京大 iPS細胞研究所(CiRA) 増殖分化機構研究部門の藤原侑哉T-CiRAプログラム研究員、同・三木健嗣特定助教兼T-CiRAプログラム研究員(研究当時、元・米 ハーバード大学兼マサチューセッツ総合病院リサーチフェロー)、同・吉田善紀准教授/T-CiRAプログラム主任研究員らの研究チームによるもの。詳細は、幹細胞研究に関する全般を扱うオープンアクセスジャーナル「Stem Cell Reports」に掲載された。
「肥大型心筋症」(HCM)は、左心室の肥大を特徴とし、500人に1人が罹患するとされる。HCMの治療法は対症療法しかなく、治療薬の開発が進んでいないことが課題となっている。その主な理由は、ヒトのHCMを正確に再現した疾患モデルがないためで、特に重症度の違いを正確に再現できていないという。そこで期待されているのが、ヒトiPS細胞を用いたECTだ。しかしECTは成体の心臓と比べて未成熟なため、HCMのより正確な病態を再現するためにはその成熟度を高める必要があった。
そこで研究チームは今回、過去の研究で見出した、心筋細胞の成熟化を促進する化合物であるエストロゲン関連受容体作動薬の「T112」を用いて成熟したECTを作製し、HCMの病態をより正確に再現する手法の確立を目指したという。
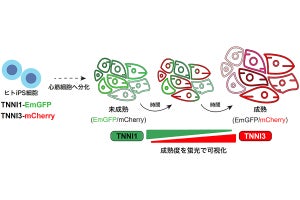
骨格筋を構成する「筋原繊維」はZ帯で仕切られており、その仕切られた単位を「サルコメア」という。HCMの約60%は、常染色体優性遺伝によるサルコメアの障害であり、1400以上の関連遺伝子変異が発見済みだ。サルコメアの「TNNI遺伝子」は、胎児型の「TNNI1」から成体型の「TNNI3」へと切り替わることが知られている。そこで今回の実験では、TNNI1が発現している時には蛍光タンパク質「EmGFP」により緑色に、TNNI3が発現している時には同様に「mCherry」により赤色に光るように遺伝子を導入したiPS細胞が利用された。
そして伸長刺激を与えることができる装置を用いて、iPS細胞から誘導されたECTの伸長を実施。するとT112処理を行ったECT(T112-static)において、成熟心筋であることを示すmCherryの発現は有意に高く、約2倍に増加したとする。さらに、T112処理と伸長刺激を行ったECT(T112-Mech.)におけるmCherryの発現は、伸長刺激を行わなかったT112-Staticにおける発現よりも有意に高く、1.6倍に増加したという。
さらに、心筋の成熟に関わるサルコメアの長さ・収縮力・ミトコンドリアDNA含有量・グルコース消費量などのさまざまな指標について、T112処理と伸長刺激の組み合わせにより、より成熟した状態になることが確認された。
次に、健常者由来のiPS細胞をゲノム編集することにより、MYH7遺伝子を変異させ、同iPS細胞からECTを作製し、HCMの病態の再現に関する確認が行われた。すると、野生型(WT)ECTでは成熟が進むに連れて筋原線維の配列の乱れ具合が改善したが、遺伝子変異を持つECT「R719Q」では調べられた全条件で改善していなかったとのこと。その結果、HCMで見られる筋原線維の配列の乱れは、T112-Mech.処理群でのみ観察されたという。
またR719QのECTでは、WT ECTよりも収縮力が高く、弛緩時間が長いという結果が見られた。成熟ECTを用いることで、重度の病態を示す遺伝子変異を持つHCMで見られる筋原線維配列の乱れ・肥大・収縮亢進・拡張機能障害を含むいくつかの特徴的なHCMの表現型の再現が実現された。
HCM患者のうち、MYBPC3切断変異は頻度が高い変異の1つだ。そこで研究チームは、健常者由来のiPS細胞(WT)に対してゲノム編集を行い、MYBPC3切断変異を持つiPS細胞株「MYBPC3G115」を作製した。WTとMYBPC3 G115からそれぞれECTを作製したところ、通常の培養条件では心筋細胞の大きさに差は見られなかったとする。ただし、T112処理と伸長刺激を組み合わせた方法では、MYBPC3G115*は肥大していることが確認され、また筋原繊維配列の乱れや収縮力・収縮時間などは同程度だったが、弛緩時間が長くなっていることも判明した。
つまり、臨床的により軽度の病態を示す病原性サルコメア遺伝子変異(MYBPC3 G115*)を持つECTにおいて、T112処理と伸長刺激を行う方法は、心筋細胞肥大のようなHCMの表現型の再現を実現したことになるとする。
研究チームは、今回作製されたECTが、HCMの治療法開発に役立つことが期待されるとしている。