プラチナバイオと広島大学の両者は9月25日、ゲノム編集の安全性を簡易的にチェックする評価ソフトウェア「DANGER analysis」を開発したことを共同で発表した。
同成果は、プラチナバイオの中前和恭主任研究員(広島大 ゲノム編集イノベーションセンター 共同研究講座助教兼任)、広島大大学院 統合生命科学研究科の坊農秀雅特任教授らの共同研究チームによるもの。詳細は、バイオインフォマティクスと計算生物学に関する全般を扱うオープンアクセスジャーナル「Bioinformatics Advances」に掲載された。
現存する地球の生物に、姓名の設計図としてDNAが用いていることは誰でも知る事実だ(生物と非生物の中間的な存在として扱われているウイルスはRNAのみのものも多い)。DNAは、アデニン(A)、グアニン(G)、シトシン(C)、チミン(T)という4つの塩基により構成されており、その4種類の組み合わせでさまざまな遺伝情報(遺伝子)が表されている。その遺伝情報全体のことをゲノムという。
ゲノム編集とはDNAの任意の塩基配列に対し、「CRISPR-Cas9」に代表される生体分子からなるゲノム編集ツールを作用させて、塩基配列の変化を誘導できる技術だ。しかし、ゲノム編集には「オフターゲット作用」という大きな問題もある。これはゲノム編集をしたい塩基配列とは異なる塩基配列に対し、意図しない変化を起こしてしまう現象だ。
これまで世界中で、オフターゲット作用を検出するためのさまざまな手法が開発されてきたが、同作用が引き起こす有害な作用を測定する定量的評価手法はまだ開発途上だった(問題1)。また、オフターゲット作用の解析には精度の高いゲノム配列情報が必要だが、高精度ゲノム配列情報の獲得には高いコストが伴うため、その解析の利用範囲は限定的だった(問題2)。
そこで研究チームは今回、ゲノム編集の安全性を簡易的に評価するための評価ソフトウェア「DANGER analysis」を開発することにし、オフターゲット作用の中でも形質に影響を与えうる発現領域上で発生したものに着目し、同作用の有害性を数値的に推定する手法を確立することにしたという。
-
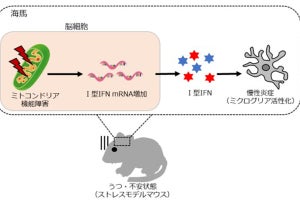
「DANGER analysis」による安全性評価の流れ。オフターゲット作用領域がゲノム編集ツールの作用を受けると予想外のRNA発現が発生する。同ソフトでは、(1)de novoトランスクリプトームアセンブリの構築、(2)発現低下領域の取得、(3)オフターゲット作用の推定、(4)(2)と(3)に基づく有害なオフターゲット作用の領域推定、(5)推定された有害なオフターゲット作用領域が属する生物機能情報を特定、(6)生物機能ごとに生体現象に対する影響リスクを数値化、という流れで解析して安全性評価が実施される。(出所:広島大プレスリリースPDF)
同ソフトでは、遺伝子発現実験データであるRNAシーケンスデータから「de novoトランスクリプトームアセンブリ」と呼ばれる手法で発現領域の塩基配列を解読し、オフターゲット作用の推定ならびに発現解析を行う仕組みだ。そして、影響を受けていると推定される遺伝情報に対して公共バイオデータベースにアクセスし、生物機能情報を取得することで、オフターゲット作用がどのような生体現象に影響を与えている可能性があるかの推定を行う。
なおde novoトランスクリプトームアセンブリとは、既知のゲノム情報を使わず、DNAシーケンサーから出力された配列情報に基づいて発現している領域の塩基配列情報を復元する手法、もしくはその復元物全体のことをいう。これは一般的に生体内に存在するRNAが長く、現在広く使われているDNAシーケンサーでは一度に全体を読むことができないためである。解読された塩基配列情報をコンピュータ上でつなげて発現している領域の塩基配列を復元するのである。
また同ソフトでは、そのde novoトランスクリプトームアセンブリを利用しているため、高精度なゲノム配列情報なしで簡易的なオフターゲット作用解析が可能だ。そのため、商品作物や患者の細胞でもゲノム編集でのオフターゲット作用の多寡と影響度を発現領域の範囲内で簡単に評価することができる(問題2の解決)。
また、同ソフトによる解析を予備調査に利用し、高精度ゲノム配列情報を用いた既存のオフターゲット解析法による精査につなげることも考えられるとしている。今回の研究成果は、世界中の品種改良やゲノム医療の安全性証明法として利用が期待されるとした。
なお、今回開発された「DANGER analysis」は、商用利用問わず誰でも無償利用できるコードとしてGitHub上に公開中だ。