東京医科歯科大学(TMDU)は6月23日、ラットを用いた動物実験で、mRNA医薬による顎骨の欠損に対する骨再生治療に成功したことを発表した。
同成果は、TMDU 生体材料工学研究所 生命機能医学分野の位髙啓史教授、同・福島雄大助教、同・中西秀之助教、同・鄧佳大学院生、同・大学大学院 医歯学総合研究科 生体補綴歯科学分野の若林則幸教授、同・野﨑浩佑講師、同・張茂芮大学院生らの共同研究チームによるもの。詳細は、「Inflammation and Regeneration」に掲載された。
骨は本来自然に治癒する能力を持つ組織だが、完治までに長い期間を要することも多い。そのため大きな骨欠損を生じた場合の対処は、依然として重大な医学的課題だという。特に顎顔面領域は、腫瘍切除、外傷などにより大きな骨欠損を生ずることがしばしばあり、機能的・美容的に深刻な問題となるが、まだその治療法を確立できていないとする。
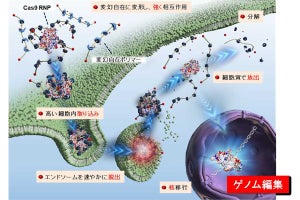
mRNA医薬を用いれば、どのようなタンパク質を投与することも可能で、組織再生に効果が期待されるタンパク質を局所的・一過性に産生させることで、再生医療への応用も期待されている。今回の研究では、顎顔面領域の骨欠損に対する治療への応用を想定し、mRNAを用いて複数の治療用タンパク質を組み合わせて投与することによる、新しい骨再生治療を試みたという。
今回の研究では、骨再生の効果を示す治療用タンパク質として、研究チームが先行研究で発見した骨誘導性転写因子(Runx2)と、血管内皮増殖因子として知られる「VEGF」の2種が用いられた。後者は、本来は血管新生に働く分泌タンパク質で、骨欠損部位への血管誘導が骨再生を促進する効果が期待されること、一方VEGF自体に骨分化誘導の機能があるとの研究報告もあり、Runx2との相乗的な効果が期待されるものとして選択したという。
まず、培養細胞(未分化骨芽細胞)に対し、それらのmRNAを投与して、骨分化誘導能を評価したとのこと。その結果、Runx2、VEGFそれぞれを単独で投与しても、「オステオポンチン」や「オステオカルシン」などの骨分化マーカーの発現が亢進し、Runx2だけでなく、VEGFも骨分化誘導能を持つことが示唆された。さらに両者を同時投与すると、より高い骨分化マーカー発現が観察され、両者が相乗的に細胞の骨分化誘導に働くことが示唆されたとする。
続いて、顎骨に径4mmの骨孔を作成したモデルラットを用いて、これらのmRNAの骨再生効果が検証された(同モデルは無治療では自然治癒しないことが知られている)。この骨欠損部へのmRNA投与には、研究チームが先行研究にて開発を進めてきたナノミセル型mRNAキャリアが応用された。具体的には、骨欠損作成後1週から、週1回の間隔で計3回のmRNA投与を行い、マイクロCTによる骨の撮影、および組織学的評価を行ったという。
結果として、Runx2、VEGFいずれかの単独投与でも、無治療群あるいはコントロールmRNA投与群と比べて、骨欠損部に良好な骨再生が得られた。さらに、細胞での結果と一致して、この両者を組み合わせて投与した群で最も旺盛な骨再生が観察されたという。新生骨を詳細に評価すると、骨量や骨石灰化量など骨の性状を示す値がこの組み合わせ投与群で最も高い値となり、旺盛な骨再生が裏付けられたとした。
骨欠損作成後4週での骨再生部位の組織学的評価では、Runx2投与群(単独またはVEGFとの組み合わせ)で、アルカリフォスファターゼ(ALP)などの骨分化マーカーが広範に発現し、一方VEGF投与群(単独またはRunx2との組み合わせ)で、血管新生マーカー(CD31)の発現の亢進が観察された。VEGF投与群でも、Runx2m投与群よりは低い程度ながら骨誘導マーカー発現が増加したことから、VEGFも骨誘導能を持つことが示唆されたという。
つまり、VEGFは骨欠損部への血管新生、骨誘導の両方の役割を果たしたことが示唆され、さらにRunx2と組み合わせることにより、両者が相乗的に作用し、より活発な骨再生を誘導したものと考えられるとしている。また、今回のmRNA投与によって、投与局所での炎症反応など、明らかな有害事象は観察されなかったとする。
mRNA医薬の再生医療への応用例は、まだわずかだ。そうした中で今回の研究により、分泌タンパク質であるVEGF、細胞内で働く転写因子のRunx2という、まったく種類の異なるタンパク質であっても、それらを自在に組み合わせて治療に用いることができるmRNA医薬の特徴が明確に示された。VEGFによって血管新生の積極的な誘導が可能となることは、特に顎顔面領域などの大きな骨欠損に対して有効に働く可能性があるといい、mRNA医薬を用いた、細胞移植を必要としない再生医療の実現に向けた重要な一歩と位置づけられるとしている。