東京大学(東大)は4月7日、高額なヒト小腸オルガノイド培養の低コスト化に向け、2018年に開発した「マウスL細胞」に、さらにタンパク質「HGF」を強制的に発現させた「L-WRNH細胞」の培養上清を用いること、さらに細胞外基質を従来のマトリゲルから安価なコラーゲンゲルへと代替することで、これまでの1/100程度という大幅なコスト削減を達成したことを発表した。
同成果は、東大大学院 農学生命科学研究科 応用生命化学専攻の高橋裕助教、同・井上優大学院生(研究当時)、和歌山県立医科大学 薬学部の佐藤慎太郎教授、東大大学院 薬学系研究科附属創薬機構の岡部隆義特任教授、同・小島宏建副機構長、千葉大学 災害治療学研究所 未来医療教育研究機構の清野宏特任教授、東大大学院 農学生命科学研究科 応用生命化学専攻の清水誠特任准教授(研究当時)、同・山内祥生攻准教授、同・佐藤隆一郎教授(研究当時)らの共同研究チームによるもの。詳細は、英オンライン総合学術誌「Scientific Reports」に掲載された。
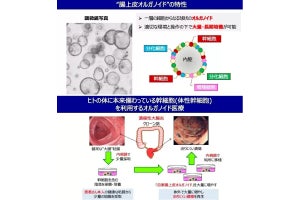
オルガノイドは、臓器特異的幹細胞およびその幹細胞から分化した細胞群を含む細胞集団であり、臓器に類似した構造、機能を有する。特にヒトオルガノイドは、ヒト生物学の解明に迫るための画期的な実験材料として期待されている。
その中でも小腸オルガノイドは、複数種類の小腸上皮細胞で構成され、正常な小腸上皮細胞の生理機能を評価するための優れた培養モデルと考えられている。ただし同オルガノイドの培養においては、すべての材料を市販品で賄って作製した場合、24-well plate1枚分で約20万円という高額なコストが課題となっていた。
研究チームはこれまで、タンパク質の「Wnt3a」、「R-spondin1」、「Noggin」を安定発現させたマウスL細胞の培養上清を培地として用いることで、ヒト小腸オルガノイドの培養コスト削減を実現してきた。しかし、大量培養を行う場合のコストは依然として高く、さらなる削減が求められていた。
そこで今回の研究ではまず、オルガノイドの培養に必要なタンパク質「hepatocyte growth factor(HGF)」を強制発現させたL-WRN細胞の培養上清を培地として採用し、マウスL細胞を用いた時と比較してコストの削減に成功した。さらに、細胞外基質を従来の「マトリゲル」から、その1/10程度の価格でありながら、増殖性や性質は大きく変化しない「I型コラーゲンゲル」に変更。これにより、トータルで当初のコストから1/100程度まで削減を実現できたとする。
さらに、これらの方法を組み合わせて培養したヒト小腸オルガノイドを用いて単層上皮細胞を得られること、また「Caco-2細胞」よりもヒト小腸オルガノイドに選択的に細胞毒性を誘導する化合物を約3500化合物の既知薬理活性ライブラリから同定することに成功したという。
そして研究チームはその中の1つ、Caco-2細胞における細胞毒性は見られず、ヒト小腸オルガノイドにのみ明確な細胞毒性が見られた「YC-1」に着目したとする。YC-1は、可溶性グアニル酸シクラーゼの活性化剤であると同時に、低酸素状態で活性化する転写因子「HIF-1α」の阻害剤でもある。
しかし、ほかの可溶性グアニル酸シクラーゼ活性化剤およびHIF-1α阻害剤を処理しても、オルガノイドに細胞毒性が誘導されなかったことから、YC-1によるオルガノイドへの細胞毒性は、これらの既知薬理作用とは異なる機序で引き起こされることが考えられたという。
また、YC-1による細胞毒性は「メサンギウム細胞」などの複数の細胞種においてこれまで報告されているが、その作用機序はMEK/ERK、p38 MAPK、c-Jun N末端キナーゼのそれぞれを介した3種類の経路が報告済みだ。そして各種阻害剤を用いた検討を行ったところ、オルガノイドにおけるYC-1の細胞毒性は、MEK/ERK経路を介することが示されたとする。
研究チームは今回の研究により、ヒト小腸オルガノイドの培養コストを当初の1/100程度まで削減することが実現され、特に継続的な使用や大規模スクリーニングなどの大量培養が必要となる場合において、少なくとも費用の観点からヒト小腸オルガノイドをより活用しやすくなったとする。さらにこのコスト削減により、オルガノイド培養のハードルが下がることで、これまでにオルガノイド研究を行っていなかった研究者も、同研究に参画しやすくなることが見込まれるとしている。