大阪大学(阪大)は3月17日、う蝕(むし歯)に継発する可逆性・不可逆性歯髄炎の病態解明に取り組んだ結果、う蝕の進行に依存して歯髄(しずい)内に特徴的な分子(白血球の一種のマクロファージ)の発現を認め、可逆性歯髄炎および不可逆性歯髄炎のラット動物実験モデルの確立に成功したと発表した。
同成果は、阪大 歯学部附属病院の高橋雄介講師、阪大大学院 歯学研究科の黄海玲特任研究員、同・林美加子教授らの研究チームによるもの。詳細は、歯科・口腔および頭蓋顔面科学の臨床研究の全般を扱う学術誌「Journal of Dental Research」に掲載された。
歯髄は歯の最も内側に存在しており、象牙質知覚過敏などで痛みを感じるなど知覚を司る組織のことで、「歯の神経」などと呼ばれる。そこでう蝕などが発生することによって誘発された炎症が、歯髄炎だ。これは主に進行したう蝕に継発して生じる病変で、激しい痛みを伴う。
可逆性歯髄炎の場合は治癒が見込めることもあるが、不可逆性歯髄炎に罹患すると、歯髄保存療法の適応が難しく、これまでは歯髄を除去する治療(抜髄)が行われてきた。しかし、歯髄を喪失した歯はその寿命が短くなるという報告も多く、抜髄はできるだけ避けるべき治療法だという。また、歯髄炎は正確な診断が難しく、可逆性と不可逆性の境界の判別が困難であり、それに伴って標準治療の設定も困難となるため、解決すべき課題とされていた。
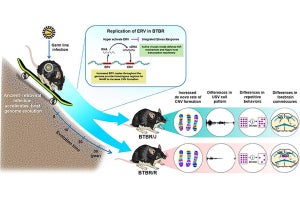
そこで研究チームは今回、可逆性・不可逆性歯髄炎の病態を解明するため、ラットにう蝕を誘発させ、その進行について詳細な画像解析を行い、病理組織学的に解析したという。その結果、軽度のう蝕では歯髄にM2マクロファージが多く出現し、重度に進行したう蝕ではM1マクロファージが多く存在することが見出されたとした。
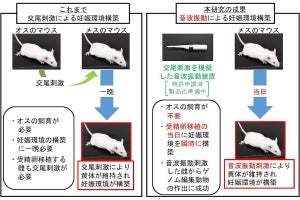
また、さまざまなう蝕の状態に対して歯髄保存療法(覆髄)を実施し、これが奏功するものを可逆性歯髄炎モデル、奏功しないものを不可逆性歯髄炎モデルとして確立することに成功したとする。さらに、可逆性歯髄炎に対して歯髄保存療法を実施した後の歯髄組織においてもM2マクロファージが多く存在し、特徴的な治癒機転を示すことが明らかになったとした。
-
これまで歯髄炎の病態については不明な点が多く、そのため歯髄炎に罹患した場合の第一選択は歯髄除去療法だった。しかし、う蝕誘発ラットの解析で再現性高く歯髄炎を惹起することに成功。さらに、可逆性・不可逆性歯髄炎を特徴づけるマクロファージの局在についても見出され、今回、歯髄炎の動物実験モデルの確立に世界で初めて成功した(出所:阪大Webサイト)
研究チームは、今回の研究成果により、世界で初めて可逆性および不可逆性歯髄炎の動物実験モデルが確立されたとする。加えて、歯髄炎を特徴づける分子の同定にも成功したため、これまで困難だった歯髄炎の正確な診断ならびに歯髄保存療法の適応が拡大されることが期待されるとしている。