auhtor=波留久泉
慶應義塾大学(慶大)は12月23日、動物の肝臓から主にコラーゲンなどの有効成分を残してバイオ臓器骨格を取り出す「脱細胞」という技術を応用して、ヒトにも応用可能な大きさのバイオ人工肝臓を作製し、動物への移植に成功したと発表した。
同成果は、慶大医学部 外科学教室(一般・消化器)/の東尚伸大学院生(慶大大学院 医学研究科)、同・八木洋専任講師、同・北川雄光教授らの研究チームによるもの。詳細は、臓器および組織の移植を扱う学術誌「American Journal of Transplantation」に掲載された。
現在、末期肝不全患者に対する治療法は移植治療のみであるが、臓器提供者(ドナー)が慢性的に不足しており、全世界で年間200万人以上の人々が肝臓疾患で死亡しているという。そのため、iPS細胞をはじめとする再生医療による臓器再生に期待がかかるが、ヒトに適用可能な大きさの臓器再生の実現には多くの課題が残されているという。
今回、研究チームは、この再生医療技術の障壁であった「大きさのギャップ」を埋める技術開発に向け、臓器から不必要な細胞を洗い流し、有効成分だけを残す手法である「脱細胞化」という手法に着目。ブタを研究対象に、肝臓から細胞外マトリックスなどの有効成分だけを残して界面活性剤などを用いて効率的に洗い流し、肝臓の骨格構造を維持する手法を確立したとする。
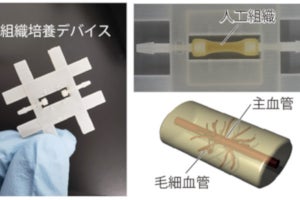
この手法を用いると、新しく外部から細胞を注入して充填した際に、コラーゲンを主体とした肝臓の骨格構造に細胞が生着しやすい環境を作り出すことが可能となったとのことで、実際に、脱細胞化処理を行った後でも多くの細胞外マトリックス成分が残存し、肝臓内部の血管・胆管の構造が保たれていることが示されたという。
実際の実験では、ブタの肝臓細胞と血管内皮細胞を、脱細胞化した肝臓骨格の内部の血管に対し、注入圧力を測定しながらゆっくりとしたペースで充填。ゆっくりと進めることで、移植肝臓としての機能を果たすために必要とされる十分な数の肝細胞と、移植後の血栓化を防ぐのに十分な血管内皮細胞を生着させることに成功。細胞が充填された後に肝臓としての機能を測定したところ、アルブミンや尿素、凝固因子という肝臓で作られる物質が検出されたほか、ほかの肝臓機能に重要な遺伝子であるCYP関連遺伝子の発現が上昇していることも確認されたことから、体外でヒトの肝臓の大きさに近く、実際に肝臓機能を発現するバイオ人工肝臓の作製に成功したと判断されたとしている。
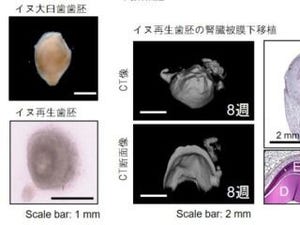
さらに、バイオ人工肝臓の治療効果の証明として、肝臓障害(慢性肝不全)を誘導したブタにバイオ人工肝臓の血管をつないだ上で、体内への移植を実施したところ、1か月間で肝臓障害を治療することに成功したとするほか、移植ブタでは非移植ブタと比較して、特に移植後の早い日数で肝機能が改善していることが、各種の肝臓関連の血液検査データから確認されたという。実際に、移植手術後2週間目と1か月目に行った、造影CTによる撮影でもバイオ人工肝臓内部に血液の流入があることが確認されたとしている。
移植手術1か月後に、バイオ人工肝臓を摘出して病理組織学的な調査を行ったところ、充填した肝細胞や血管内皮細胞が内部でしっかりと生存しており、一部では新しく胆管の構造が作られて、胆汁も産生され始めていることも判明したほか、人工肝臓内部で、正常の肝臓で見られるような遺伝子発現も認められたという。
今回の成果は、今後の臓器再生医療の実現化に向けて大きな進歩だと研究チームでは説明しており、今回と同じ方法でヒトiPS細胞から作られた細胞を充填する研究も進められているとする。そのため、近い将来、肝不全を治療できるヒトバイオ人工肝臓の完成とともに、ほかの臓器への応用も期待されるとしている。