東京大学(東大)と科学技術振興機構(JST)は11月17日、核酸やタンパク質といった無生物材料のみを用いて、生物の特徴であるDNAからの遺伝子発現と持続的な複製による進化を細胞外で行うことに成功したと発表した。
研究はJST戦略的創造研究推進事業として行われ、東大大学院 総合文化研究科 広域科学専攻・附属 先進科学研究機構 生物普遍性連携研究機構の市橋伯一教授らの研究チームによるもの。詳細は、合成生物学と生物システムを扱う学術誌「ACS Synthetic Biology」に掲載された。
生物として、自ら増殖できることと、進化の仕組みを備えていることは大きな特徴といえる。人類も、さまざまな動植物の品種改良を行うことで、より収穫量の多い食料や安価な医薬品の生産技術などを生み出してきた。しかし、生物は人間が利用するために誕生・進化してきたわけではないため、すべての面で人間に都合よく利用できるとは限らないという側面もある。
もし目的に沿った、増殖・進化の仕組みを持つ人工分子システムを作り出すことができれば、今まで生物に依存していた有用物質生産をより効率的かつ安定的に行えることが期待されることになるが、そのためには、DNAの複製を何世代にもわたって長く続けられる仕組みであったり、その複製においても、DNAに書かれている情報(遺伝子)を翻訳してタンパク質を発現させ、そのタンパク質によってDNAを複製することを可能とする必要があり、現在までに、そうしたDNA複製に必要な遺伝子の発現とそれによるDNA複製が同時に起こる反応系構築は達成されていない。
DNA複製に必要な遺伝子の発現と、それによるDNA複製を同時に起こすためには、多数のDNA複製に必要な遺伝子を十分な量で供給する必要があるが、それが難しいためである。
そこで研究チームは、生物が使っているような、精巧だが多数の遺伝子を必要とする複雑なDNA複製機構ではなく、もっと少ない遺伝子で、なおかつ低濃度のタンパク質で達成可能なDNA複製の仕組みを人工的に作ることにしたという。
今回用いられたDNA複製の仕組みでは、「Phi29DNA複製酵素」と「Cre組み換え酵素」という2種類の遺伝子を利用することで、再帰的な環状DNA(人工ゲノムDNA)の複製を実現したという。またその2つのタンパク質も低濃度で十分機能し、現在の無細胞翻訳系でも十分な量を発現できることが予想されたという。
-
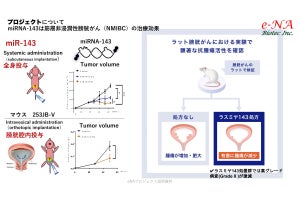
人工的に設計されたDNA複製の仕組み。DNAから2種類のタンパク質が発現し、Phi29DNA複製酵素によって環状DNAから2本鎖の長い直鎖状DNAが合成される。その後、Cre組み換え酵素により分子内で相同組み換えが起こり、環状DNAが再生される。このような仕組みは海外の研究者によって提案されていたが、Cre組み換え酵素がDNA複製酵素の機能を強く阻害してしまうため、長年実現されていなかった。研究チームの2018年の研究により、阻害効果が少ないDNA複製酵素変異体が取得され、今回の研究が実現した (出所:プレスリリースPDF)
さらに、この人工ゲノムDNAを持続的に複製できるかどうかが人工ゲノムDNAの無細胞転写翻訳系での反応として検証された結果、8回継代後にはDNAがまったく増えなくなったという。理由としては、複製中に複製エラーにより遺伝子の機能を壊してしまう変異が入り、複製を繰り返していくと、いつかは遺伝子が完全に壊れてしまうためで、壊れた遺伝子を持つDNAを除く方法として、直径0.5~0.8μmの油中水滴による区画構造を導入し、細胞当たりのゲノムDNAの数を少数(できれば1個)に限定する手法を考案。水滴中に、人工ゲノムDNAと無細胞転写翻訳反応液を封入した実験を改めて行ったところ、8ラウンド経過後も複製が持続することが確認されたという。また、当初は徐々にDNA濃度が低下する傾向にあったが、18ラウンドになると急によく増えるようになり、60ラウンド(60日間、140世代相当)までDNA複製を続けることができたという。
-
区画構造がない条件で継代した場合のDNA濃度の推移。8、9ラウンドではDNA複製が起きなくなった。6ラウンド(黒矢じり)では、DNA濃度が検出感度以下になったため、一度DNAを取り出して人為的に増幅したのち、再び区画内に戻されている (出所:プレスリリースPDF)
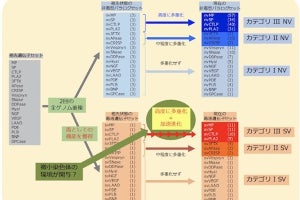
30ラウンド時点でDNAを18個単離し、その配列を調べたところ、平均7個の変異が入っていることが確認され、そのうちの5個は過半数のDNAに共通していたという。また単離された多くのDNAの複製能力は、元のDNAに比べて最大で約10倍まで上昇していることが判明。このことは、適応進化が起きたことが示されていると研究チームでは説明している。
なお、今回の研究では、DNA複製に必要な2遺伝子だけが用いられたが、そこにほかの遺伝子を導入することも可能で、それによって人工ゲノムDNAの持つ機能を拡張していくことができるという。それにより、RNAやタンパク質もゲノムDNAから発現させることができるため、今後、転写翻訳に必要な遺伝子をすべて載せれば、アミノ酸や塩基などの低分子化合物を与えるだけで自律的に増殖をする人工分子システムへと発展させることができるとするほか、膜合成遺伝子を導入すれば、細胞膜を作り出せる可能性もあるとしている。
-
区画構造がある条件で継代したときのDNA濃度の推移。(A)油中水滴中での反応が行われ、次のラウンドでは新しい無細胞転写翻訳反応液を含む油中水滴で希釈され、かき混ぜることで水滴の中身が混ぜて反応させられた。(B)各ラウンドでDNA濃度が測定された。独立した2系統の実験が行われ、どちらも複製は最後まで持続した(グラフはそのうちの1例のもの)。黒矢じりで示されているラウンドでは、DNA濃度が検出感度以下になったため、一度DNAを取り出して人為的に増幅したのち、再び区画内に戻されている (出所:プレスリリースPDF)
さらに、翻訳したタンパク質の機能が十分でなければ、進化させることでその機能を向上させることも可能であり、今回の人工ゲノムDNAをコアにすることで、自律的に増殖する人工細胞の構築につながることが期待されるとしている。