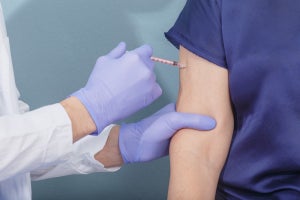
ファイザーは8月16日(米国時間)、同社とBioNTechが提供する新型コロナウイルス感染症(COVID-19)向けワクチン(BNT162b2)の3回目接種(ブースター)に関する初期臨床試験(治験)結果を米食品医薬品局(FDA)に提出したことを発表した。
それによると、米国の成人参加者における新型コロナワクチンの3回目の投与の安全性、忍容性、および免疫原性を評価する今回の試験は、2回目の投与を受けてから8〜9か月後に30μgの投与を行う形で実施。その結果、2回目の接種直後に比べて、中和抗体の力価が従来株のみならず、デルタ株、ベータ株に対しても有意に増加したことが確認されたという。
今回の成果を踏まえファイザーでは、当初の2回のワクチン接種後6〜12か月以内に追加接種を行うことで、新型コロナに対する高い予防効果を維持するのに役立つ可能性があるとしている。
なお、今回のデータについては、FDAのみならず、今後数週間以内に欧州医薬品庁(EMA)およびその他の規制当局にも提出される予定だという。また、日本政府も追加接種分の確保に動いており、ファイザーとの間で1億2000万回分の追加契約を交わす方向で調整を進めているとしている。