京都大学iPS細胞研究所(CiRA)、タケダ-CiRA 共同研究プログラム(T-CiRA)、日本医療研究開発機構(AMED)の3者は6月21日、約9000種類の化合物から、「エストロゲン関連受容体γ(ERRγ)作動薬」がヒトiPS細胞由来心筋細胞の成熟を促進することを発見したと発表した。またERRγ作動薬を用いることで、従来は胎児レベルまでだった心筋細胞を、T管構造を有する新生児レベルにまで成熟させることに成功したことも合わせて発表された。
同成果は、CiRA 増殖分化機構研究部門の三木健嗣特定助教兼T-CiRAプログラム研究員(現・ハーバード大学兼マサチューセッツ総合病院リサーチフェロー)、武田薬品工業の出口康平リサーチ兼T-CiRAディスカバリー主任研究員、CiRA 増殖分化機構研究部門兼T-CiRAプログラムの小圷美聡研究員、武田薬品工業の西本誠之リサーチ兼T-CiRAディスカバリー主席研究員、CiRA 増殖分化機構研究部門の吉田善紀准教授兼T-CiRAプログラム主任研究員らの共同研究チームによるもの。詳細は、英オンライン科学誌「Nature Communications」に掲載された。
ヒトiPS細胞を含む多能性幹細胞由来の心筋細胞は、さまざまな心疾患研究や薬剤試験、再生医療への応用が期待されている一方で、従来、分化して得られる心筋細胞は胎児レベルのもので、成熟度の面で課題を抱えていたという。
そこで研究チームは今回、心臓発生において心筋細胞の成熟度に伴い変化するタンパク質「トロポニン」の移り変わり(胎児型:TNNI1、成人型:TNNI3)に着目。これら2つのタンパク質の量に応じて蛍光する「ダブルレポーターヒトiPS細胞」を作製し、心筋細胞の成熟度を可視化することを試みたという。
-
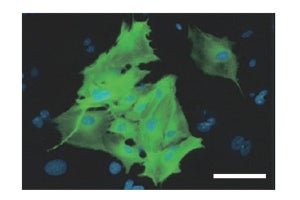
ダブルレポーターヒトiPS細胞の特性についての概要図。EmGFPおよびmCherryのレポーター遺伝子が挿入されたヒトiPS細胞株は、心筋細胞へ分化させると、成熟度により緑色から赤色の蛍光を示す (出所:CiRA Webサイト)
実際に、ダブルレポーターiPS細胞株が用いられ、約9000種類の化合物の中からTNNI1からTNNI3へのトロポニンの移り変わりを促進する化合物の探索が行われた。その結果、「ERRγ作動薬(T112)」および「SKP2阻害薬(T623)」が、ヒトiPS細胞由来心筋細胞において毒性が低く、TNNI3へのタンパク質の移り変わりを促進する化合物であることが見出されたという。
-
ダブルレポーターヒトiPS細胞由来心筋細胞を用いた化合物スクリーニング。TNNI3-mCherryの発現が調べられたところ、T112、T623およびCombo(T112とT623が混合させられたもの)がTNNI3へのタンパク質の移り変わりを促進する化合物であることが見て取れる。スケールバーは500μm (出所:CiRA Webサイト)
また、心筋細胞の成熟化の重要な指標の1つである代謝機能についての調査も行われたところ、エストロゲン関連受容体γ(ERRγ:T112)処理群および併用群では基礎呼吸、最大呼吸、ATP(アデノシン三リン酸)産生において有意にミトコンドリア活性上昇が確認されたが、併用による相加効果は認められないことから、T623は代謝機能の向上には寄与していない可能性が示されたとする。
-
ミトコンドリア活性(OCR:酸素消費速度)の解析結果。細胞の酸素消費速度を測定することによって、細胞のミトコンドリア機能の評価が可能となる。T112処理群および併用群(Combo)では基礎呼吸、最大呼吸、ATP産生においてミトコンドリア活性の上昇を有意に確認することができる。なお、「****」は「P<0.0001」を示している (出所:CiRA Webサイト)
そこで化合物処理による心筋細胞の収縮機能の解析が行われた結果、T112処理および併用群においては、収縮や弛緩速度などの機能が有意に上昇することが判明したほか、電気生理学的解析においても、T112処理群においては活動電位の振幅などの値の上昇が確認されたという。
さらに成熟した心筋細胞の1つの特徴として挙げられるT管構造の有無の調査も実施。その結果、T112および併用群においてT管構造が認められたほか、Z帯やM帯、I帯といった成熟心筋で認められる「サルコメア構造」が確認されたという。一方、コントロール(DMSO)群およびT623群においてはT管構造およびM帯は認められなかったという。
-
T112処理したヒトiPS細胞由来心筋細胞の電子顕微鏡画像。略称のTTはT管構造、ZはZ帯、IはI帯のこと。サルコメア長はZ帯で仕切られた間の距離で測定される。サルコメアの中には2つのフィラメントが存在し、太いものがミオシン、細いものがアクチン。これらのフィラメントがお互いに滑り込むことによってサルコメアが収縮する。収縮前、細いフィラメントのみで構成される部分をI帯、細いフィラメントと太いフィラメントで構成される部分をA帯と呼び、A帯の中央には微細な横線の帯(M帯)が見える。スケールバーは500μm (出所:CiRA Webサイト)
加えて、サルコメアの長さ解析が行われた結果、DMSO群に比べて化合物処理群において有意な増加が認められ、T112および併用群が最も長いサルコメア長を有していることが判明。これらの結果より、T112はヒトiPS細胞由来心筋細胞を、T管構造を有するレベルにまで成熟させることが確認されたとする。
これらの結果を踏まえ、ERRγを欠損したヒトiPS細胞の作製を行い、その心筋細胞がT112により成熟するかどうかのメカニズム解析が行われた。その結果、ERRγ欠損ヒトiPS細胞株由来の心筋細胞では、T112を添加してもTNNI3-mCherry陽性細胞の上昇は認められなかったとするほか、ミトコンドリア活性の解析においても、DMSOと同様に基礎呼吸、最大呼吸、ATP産生の上昇は認められなかったことから、T112はERRγを介してTNNI3の発現上昇や代謝機能を促進していることが示されたという。
-
ERRγ欠損ヒトiPS細胞由来心筋細胞を用いたT112の効果の検証。(a)化合物スクリーニングにおいて、T623を添加すると若干のTNNI3-mCherry陽性細胞が認められるのに対し、コントロール(DMSO)およびT112においてはTNNI3-mCherry陽性細胞は認められない。(b)ミトコンドリア活性(OCR:酸素消費速度)の解析。T112ではDMSOと同様に基礎呼吸、最大呼吸、ATP産生の上昇は認められない (出所:CiRA Webサイト)
これまで立体組織作製法などにより、T管構造を持つ心筋細胞が作製された報告はあったが、通常の平面培養において化合物を作用させるだけでT管構造を持つ成熟心筋細胞が作製されたのは初めてのことだという。また、ERRγが成熟過程において重要な役割を果たしており、その作用を化合物で増強させることにより心筋細胞の成熟化を誘導させられることが見出された点も重要な成果だと研究チームでは説明する。
なお、成人の心筋細胞はTNNI3のみが発現する細胞だが、今回作製された心筋細胞は、TNNI1とTNNI3の両方が発現している新生児のものに相当する心筋細胞であるという。今後、研究チームでは、成熟が進んだ心筋細胞を用いることで、これまでに表現型を認められなかった疾患モデルの構築やその創薬研究、さらに成熟心筋細胞を用いた薬理試験や細胞治療などの研究が発展すると共に、成人レベルの心筋細胞への成熟化の研究などに発展することなどが期待されるとしている。