立命館大学は4月23日、持久系スポーツのアスリートに発生する不整脈の1つである「房室ブロック」の分子メカニズムとして、「心臓イオンチャネルタンパク質」の機能障害を突き止め、さらにタンパク質をコードしない遺伝子DNA領域から生成されるマイクロRNAが関与していることを解明したと発表した。
同成果は、立命館大 生命科学部 幹細胞・再生医学研究室の中尾周講師(現・応用分子生理学研究室)、英・マンチェスター大学のMark Boyett教授、同・Alicia D'Souza博士、さらに仏・モンペリエ大学、デンマーク・コペンハーゲン大学、オランダ・マーストリヒト大学の研究者も参加した国際共同研究チームによるもの。詳細は、米国心臓協会誌「Circulation Research」に掲載された。
アスリートといえばその鍛えられた肉体から、健康そのもののイメージが強い。しかし、身体に大きな負荷をかけているのも事実で、たとえば持久系のスポーツでは、心拍数の異常(不整脈)を引き起こす場合があることが知られている。
中でも、心房と心室の連動が悪くなる房室ブロックという不整脈の発生頻度は高いという。中には、選手が晩年になってから治療が必要なほど悪化してしまうこともあるというアスリートにおける不整脈は、自律神経(特に副交感神経)の活動、つまり心臓の外側に原因があるのではないかと長年考えられてきたが、その詳細な原因メカニズムは不明だった。
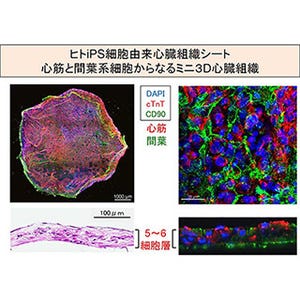
そうした背景を踏まえ、研究チームは今回、房室ブロックの分子メカニズムを明らかにすることを目的に、運動させたマウスおよびトレーニング歴のあるウマを不整脈モデル動物として用いた動物個体から分子レベルにおよぶ多角的な解析を実施したという。
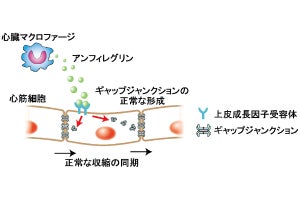
その結果、持久運動によって心臓ペースメーカー機能の低下したマウスおよびウマのいずれにおいても、心房と心室をつなぐ唯一の電気的な伝導経路である「房室結節」において、心筋細胞の電気活動を制御するイオンチャネルタンパク質、特に「Ca2+チャネル」および「ペースメーカーチャネル」の量的および機能的低下が生じていることが確認され、タンパク質をコードしない遺伝子DNA領域から作られる「マイクロRNA」の「miR-211-5p」および「miR-432」が関与している可能性が示されたという。
今回の研究成果は、人間のアスリートに発生する不整脈の根本原因となる新たな分子メカニズムを提唱するもので、見出されたマイクロRNAを抑制する方法の開発は、運動によって引き起こされる不整脈の新たな治療選択肢として、機械式ペースメーカー移植治療を受けるリスクの低下に貢献することが期待されると研究チームでは説明している。
また、心臓の中でも拍動数を司る心臓刺激伝導系は、ユニークかつ特殊な分布や機能のために研究が難しい組織であるため、持久運動以外にもさまざまな心疾患や遺伝子異常によって、心臓刺激伝導系が原因と考えられる不整脈が発生するともしている。立命館大の中尾講師は、今後もこの興味深い心臓刺激伝導系を研究対象に、病気につながる現象を突き止め、分子標的治療や再生医療などへの応用を目指していきたいと考えているとコメントしている。