岐阜薬科大学ならびに岐阜大学は、脳腫瘍「グリオブラストーマ」の治療において、「がん幹細胞」を退治して“がんの根治”も可能な新規の創薬ターゲットを発見したと発表した。
同成果は、岐阜薬科大 大学院薬科学専攻の深澤和也大学院生(日本学術振興会特別研究員)、同・堀江哲寛大学院生(日本学術振興会特別研究員)、岐阜薬科大 薬理学研究室および岐阜大大学院 連合創薬医療情報研究科の檜井栄一教授を中心に、京都薬品工業、金沢大学、東京大学などの研究者を加えた共同研究チームによるもの。詳細は、英国学術雑誌「Oncogene」に掲載された。
グリオブラストーマは、悪性度の高いがんの一種であり、確定診断後の平均余命は14ヶ月程度だという。グリオブラストーマは、脳組織に染み込むように広がっていくため、手術により完全に取り除くことができないという厄介な特徴を持つ。また、手術後に抗がん剤投与や放射線治療を行ったとしても、2年生存率は3割以下とされており、治療成績は数十年もの間、大きな改善は見られていない。
近年の研究から、「がん幹細胞」が治療後も体内に残ってしまうことが、治療を難しくしている原因の1つであることがわかってきている。がん幹細胞は、幹細胞とあるように、分裂してがんを作り出すがんの親玉的存在だ。またがん幹細胞は、抗がん剤や放射線に対して治療抵抗性を持つことが知られている。
しかし逆にポジティブに考えれば、がん幹細胞を制圧することができれば、グリオブラストーマの治療成績を向上させることが期待することができる。しかし、がん幹細胞についてまだその全貌は明らかになっておらず、その機能がどのようにして制御されているのかについてさらなる研究が必要な状態だ。
そこで共同研究チームは、まず「バイオインフォマティクス解析」の手法を用いて、グリオブラストーマ患者の腫瘍組織の解析を実施。その結果、リン酸化酵素の遺伝子グループの1つである「CDK」遺伝子の8番目である「CDK8」の発現が増加していることが判明。CDK8は、近年、白血病や大腸がんなど、さまざまな岩との関連が報告されている遺伝子だ。
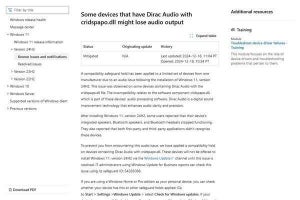
続いて共同研究チームは、グリオブラストーマ患者に由来するがん幹細胞のCDK8の働きを抑えることによって(=CDK8不活性化細胞の作製)、がん幹細胞におけるCDK8の役割を明らかにすることを試みた。その結果、がん幹細胞の機能の指標である「スフィア形成能」が低下することが確認されたという。
さらに、マウスに対してCDK8不活性化細胞の移植が行われた結果、腫瘍はほとんど確認されず、観察期間中に死亡例は1例も出ることはなかったとした。以上の結果から、がん幹細胞の腫瘍形成能にはCDK8が重要であることが確認されたのである。
次に共同研究チームは、「どうしてCDK8の働きを抑えると、がん幹細胞の機能が低下するのか?」という疑問の解決に挑むことにした。CDK8不活性化細胞について、詳細な解析を行ったところ、がん幹細胞の機能を調節しているタンパク質「c-MYC」の発現が低下していることが明らかとなった。したがって、CDK8はc-MYCの発現を調節することで、がん幹細胞の機能を制御していることが考えられるという。
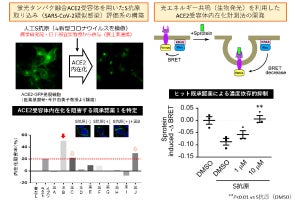
また共同研究チームは、今回の研究で得られた知見を臨床現場に還元することを目指し、「CDK8の働きを抑える薬を使って、グリオブラストーマの症状を抑えることができるか?」という課題にも挑戦。そして、独自の新規CDK8阻害剤「KY-065」の開発に成功した。
KY-065をがん幹細胞に作用させると、スフィア形成能が低下することが判明。さらに、KY-065を作用させたがん幹細胞をマウスに移植したところ、マウスの生存期間が著しく改善されたという。これらのことから、CDK8阻害剤KY-065は、新規グリオブラストーマ治療薬、およびがん幹細胞そのものに対する有望な創薬ターゲットとなる可能性があることが細胞・生体レベルで示唆されたとする。
最後に、今回の研究で得られた知見と臨床データとの関連を明らかにすることが試みられ。バイオインフォマティクス解析による大規模臨床データの解析が行われ、CDK8の発現が増加しているグリオブラストーマ患者では生存率が低下していることが確かめられた。
共同研究チームは今後、今回開発されたKY-065と既存薬のテモゾロミド、あるいは放射線療法とを併用することで、さらに治療効果を高めることができるかどうかを検討していきたいと考えているとした。
また、今回の研究成果はグリオブラストーマに限らず、がん幹細胞が悪性化に寄与するさまざまな難治性がんに対する革新的治療法を提供し、アンメット・メディカル・ニーズ(未だに有効な治療方法が確立されていない疾病に対する医療への要望)の解消にも貢献することが期待されるとしている。