理化学研究所(理研)は2月10日、毛髪を作り出す器官である「毛包」の再生能力を維持したまま毛包幹細胞を生体外で100倍以上増幅する培養方法を確立し、さらに長期間にわたる周期的な毛包再生に必要な幹細胞集団を明らかにしたと発表した。
同成果は、理研 生命機能科学研究センター 器官誘導研究チームの辻孝チームリーダー、同・武尾真上級研究員らの研究チームによるもの。詳細は、英オンライン総合学術誌「Scientific Reports」に掲載された。
ヒトなどの哺乳類の器官は、胎児期において器官誘導能を持つ「上皮性幹細胞」と「間葉性幹細胞」というふたつの幹細胞の相互作用により形成され、出生後は「体性幹細胞」によって維持される。体性幹細胞は器官誘導能を持たないため、病気やケガ、老化によって器官が機能不全に陥っても、それを再生することは不可能だ。
-
ヒトなどの哺乳類における器官や臓器の発生および維持の概念図。器官や臓器は完成すると、体性幹細胞によって維持されるが、体性幹細胞は器官誘導能を持たないため、加齢や病気、ケガなどで器官や臓器が機能不全に陥ると、再生することは叶わない (出所:理研Webサイト)
そこで現在研究が進められている次世代の再生医療は、複数の細胞種からなる器官や臓器を丸ごと再生させ、機能不全に陥った器官と置き換える「器官置換再生医療」が目指されている。器官再生医療の研究トレンドとしては、胎児期の器官誘導能を持つ幹細胞から器官の基となる「器官原基」を再生して器官へと発生させる方法と、ES細胞やiPS細胞などの多能性幹細胞に位置情報を与えてさまざまなミニ器官を誘導する「オルガノイド」の研究が進められている。
研究チームも2007年には、胎児性上皮性幹細胞・間葉性幹細胞を三次元的に操作する「器官原基法」を世界で初めて開発し、外胚葉性器官である歯や毛包、分泌腺の再生器官原基を生体内に同所的に移植して機能することを実証した。
毛髪を作り出す器官である毛包は、哺乳類において生涯にわたり再生を繰り返す唯一の器官だ。毛包は、皮脂腺や毛包上皮性幹細胞が存在するバルジ領域を含む不変部と、毛髪を作り出す工場である毛球部を含む可変部に分けられ、可変部はマウスでは約3週間、ヒトでは5~7年周期で退縮と再生を繰り返し(毛周期)、毛髪が生え変わる。
-
毛包の再生と退縮の概念図。毛包は、皮脂腺や毛包上皮性幹細胞が存在するバルジ領域を含む不変部と、毛髪を作り出す毛球部を含む可変部に分けられる。可変部は生涯にわたって退縮と再生を繰り返す。Blimp1陽性細胞(紫)は皮脂腺の維持を、Lgr5陽性細胞(緑)は可変部の再生を担う。バルジ領域のCD34とCK15の二重陽性細胞(赤)はBlimp1陽性細胞とLgr5陽性細胞を生み出す。バルジ領域と毛乳頭細胞(青)が相互作用することで毛包器官が再生される (出所:理研Webサイト)
この過程において、毛包上皮性幹細胞と毛乳頭細胞(間葉性幹細胞を含む)が相互作用することで毛包器官が再生される。これは、毛包上皮性幹細胞および間葉性幹細胞が出生後も器官誘導能を維持していることを示しており、次世代器官再生医療である毛包再生医療のための細胞ソースとして期待されているのである。
毛包は、皮脂腺の維持を担う細胞や可変部の再生を担う細胞、両者を生み出す細胞など、機能の異なる複数の幹細胞によって維持、再生される仕組みだ。それぞれの幹細胞の維持や増殖、分化に関わる分子メカニズムは明らかにされつつあるものの、周期的な毛包再生を可能とするメカニズムは明らかになっていなかった。そのため、周期的な毛包再生を可能とする幹細胞を増幅する方法は確立しておらず、毛包再生医療実現のための大きな課題となっていたのである。
そこで研究チームは今回、毛包器官誘導能の異なる毛包上皮性幹細胞の培養条件を開発。これらの培養細胞集団を比較することにより、長期間の再生の維持に必要な幹細胞集団を明らかにすることに取り組むことにしたという。
まず周期的な毛包再生に必要な幹細胞集団を明らかにするため、生体外でさまざまな培養方法が試みられた。初めに、毛包上皮性幹細胞の維持や増殖に関連するシグナル経路に関わるサイトカインや低分子化合物、培養足場材料などの組み合わせについて、220通り以上の培養条件が検討された。
-
未分化状態を維持する毛包上皮性幹細胞培養法の確立。(a)毛包バルジ細胞の立体培養イメージ。(b)培養6日目における位相差顕微鏡像(左)と細胞増殖率(右)。NFFSE培地においてバルジ細胞は最も高い増殖率を示す。(c)毛包上皮性幹細胞分布の模式図。(d)培養前後におけるCD34およびItg6発現細胞の解析。CD34/Itg6二重陽性細胞の割合はいずれの培養条件においても増加するが、NFFSE培地で最も高い割合を示すことが確かめられた。(e)培養後の遺伝子発現解析。NFFS培養細胞では毛包下部のマーカーであるLgr5の発現が、NFFSWN培養細胞では毛包上部のマーカーであるBlimp1の発現が上昇している。スケールバーはすべて100μm(1μm=1000分の1mm) (出所:理研Webサイト)
その結果、BMPシグナルを抑制するNoggin、線維芽細胞増殖因子(FGF)、HHシグナルを活性化させるSAG、上皮成長因子(EGF)を含む培地(NFFSE培地)で、アテロコラーゲンゲルを用いて立体培養すると、毛包器官誘導能を持つ上皮性幹細胞が最も高い増殖率を示し、6日間の培養で約190倍にまで増幅できることが確認されたという。
また、蛍光活性化セルソーティング(FACS)による増幅細胞集団の解析では、バルジ領域幹細胞のマーカーであるCD34/Itg6(インテグリン6)二重陽性細胞が全体の4%から70.8%に増加することが認められたとした。
一方で、この培地からEGFを除いた培地(NFFS培地)やWntシグナルおよびNotchシグナルを活性化させるサイトカインを加えた培地(NFFSWN培地)では、CD34/Itg6二重陽性細胞の割合がそれぞれ56.2%および30.6%と、NFFSE培地に比べて低い増加率となることがわかった。
そしてNFFS培養細胞では、毛包下部の再生を担う幹細胞のマーカーであるLgr5の発現が137.6倍、NFFSWN培養細胞では、皮脂腺幹細胞のマーカーであるBlimp1の発現が9.01倍まで上昇していることが判明。これらのことから、NFFSE培地が器官再生能のある毛包上皮性幹細胞を未分化状態で維持しながら増幅することが示唆されたとした。
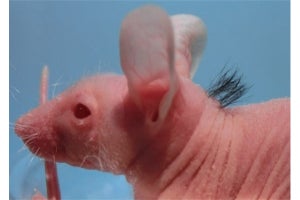
そこで培養細胞の器官誘導能を明らかにするため、器官原基法により毛包原基を再生し、ヌードマウス皮内へ同所的に移植が行われた。すると、NFFSE培養細胞およびNFFS培養細胞を用いた再生毛包原基から、同程度の毛包再生(再生毛の萌出)が確認されたという。
-
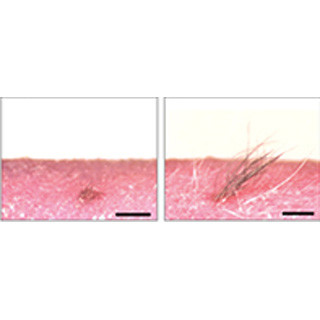
器官原基法による培養細胞の機能解析。(a)培養毛包上皮細胞および毛乳頭細胞を用いた器官原基法の模式図。コラーゲンゲル内において2種類の細胞を高密度で立体的に区画化し配置することにより、器官の基となる器官原基を再現することが可能となる。(b)ヌードマウスの皮膚内に再生毛包原基を移植して19日目の実体顕微鏡像と、発毛率および3回以上の毛周期を示す再生毛包の割合。NFFSE培養細胞から再生した毛包の多く(81.0%)が3回以上の毛周期が示された (出所:理研Webサイト)
周期的な毛包の再生回数には違いが認められ、NFFS培養細胞では79.0%の毛包が2回以下の毛周期しか示さなかったのに対し、NFFSE培養細胞から再生した毛包の81.0%が3回以上の毛周期を示したとした。このことから、長期的な毛包再生を可能とする毛包上皮性幹細胞の誘導には、NFFSE培養が重要であることが示されたのである。
研究チームはこれらの成果により、周期的な毛包再生能を持つ毛包上皮性幹細胞の生体外培養方法の確立に成功。この培養方法を応用することで、ヒト頭髪バルジ由来細胞が1毛包から4000倍に増幅され、同一期間内に毛乳頭細胞が約100倍に増幅されることから、最終的に1毛包から約100毛包相当までの増幅が可能となり、毛包再生医療の臨床応用の実現に大きく前進したとした。
以上の結果を受けて研究チームは、NFFSE培養細胞中には持続的な毛包再生を可能とする幹細胞集団が含まれていると予想。続いて、その細胞集団を明らかにするため、NFFSE培地で培養した細胞集団と、限定的な毛周期を示すNFFS培地で培養した細胞集団に対し、細胞表面マーカーの発現を用いて両者の特徴の比較が行われた。
一般的に、幹細胞の自己複製には細胞外分子群が重要な役割を果たしていることから、まず細胞接着分子および細胞外基質の発現が比較された。すると、NFFSE培養細胞集団には、バルジ幹細胞であるCD34/Itg6二重陽性細胞集団中にインテグリン5(Itg5)を高発現する細胞集団が含まれることが明らかとなった。
-
培養後の細胞集団解析とCD34/Itg6/Itg5三重陽性細胞の機能試験。(a)培養細胞の細胞表面マーカー解析。NFFS培地が0.7%なのに対し、NFFSE培養細胞は3%と、CD34/Itg6/Itg5三重陽性細胞の割合が高いことがわかる。(b)NFFSE培養細胞の発毛機能解析。NFFSE培養細胞集団からCD34/Itg6/Itg5三重陽性細胞を除去すると3回以上の毛周期を示す再生毛包の割合が79.9%から13.3%まで大きく減少することから、三重陽性細胞が周期的な毛包再生に必要であることが明らかとなった (出所:理研Webサイト)
そのうえで、NFFSE培養細胞からCD34/Itg6/Itg5三重陽性細胞を除去したうえで機能解析が行われ、3回以上の毛周期を示す再生毛包の割合が79.9%から13.3%へと大幅な減少が認められた。また細胞系譜解析では、再生毛包において三重陽性細胞は皮脂腺、バルジ領域、および毛球部を含む毛包可変部に分化することが示されたという。これらの結果から、再生毛包においてCD34/Itg6/Itg5三重陽性細胞が、周期的な毛包再生に必要であることが示されたのである。
培養実験で観察されたCD34/Itg6/Itg5三重陽性細胞の毛包における局在を明らかにするため、続いては免疫染色による解析が実施された。すると、マウスおよびヒト頭髪毛包では、サイトケラチン15(CK15)陽性バルジ領域の上部においてItg5発現細胞の局在が確かめられた。また、この領域においてEGF様ドメインを持ち、細胞接着分子のインテグリンと結合する細胞外基質の糖タンパク質である「テネイシン」の発現が確認されたという。
-
免疫組織染色によるItg5陽性細胞の天然毛包における局在解析。(a)免疫染色による天然毛包における空間的タンパク発現解析。マウス頬ヒゲ毛包、マウス体毛毛包、およびヒト頭髪毛包において、Itg5陽性細胞(緑)はCK15陽性バルジ領域上部に存在し(上段)、テネイシン(TN-CおよびTN-N)とともに局在していることがわかる(中下段)。矢尻はItg5、TN-CまたはTN-N発現領域を示す。スケールバーはすべて50μm。(b)マウス天然毛包におけるItg5陽性細胞およびテネイシン分布の模式図。CK15陽性バルジ細胞に機能的な多様性が存在し、Itg5陽性細胞が長期間の毛周期の維持に必要であり、テネイシンがItg5陽性細胞のニッチとして機能している可能性がある (出所:理研Webサイト)
これらの結果から、天然毛包においてCK15陽性バルジ細胞に機能的な多様性が存在し、Itg5陽性細胞が長期間の毛周期の維持に必要であり、テネイシンがItg5陽性細胞のニッチとして機能している可能性が示されたとした。
今回の研究により、周期的な毛包再生能を維持したまま毛包上皮性幹細胞を増幅できる培養方法の開発に成功するとともに、長期間の器官誘導能力の維持にはCD34/Itg6/Itg5三重陽性細胞が重要であることが解明された。
今回の成果は、毛包上皮性幹細胞の周期的な毛包再生や分化、運命決定のメカニズムや、上皮性幹細胞間の細胞系譜の理解などの幹細胞生物学研究に大きな貢献するとともに、「なぜほとんどすべての体性幹細胞は器官誘導能を失っているのか」、「どうしたら組織幹細胞においても器官誘導能を維持できるのか」という、発生生物学上の根本的な問いに答える足掛かりになることが期待できるとしている。
また今回の研究により確立された培養方法を応用することで、少数の毛包から大量の再生毛包を人為的に製造することが可能だ。それにより、世界初の器官再生医療である毛包器官再生医療(毛髪再生)の実現に大きく貢献することが期待できるとも、研究チームはコメントしている。