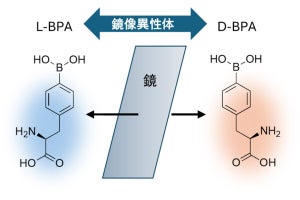
東北大学は1月4日、父親の加齢が子どもの神経発達障害様行動異常の原因となりうること、またその原因となる分子病態基盤として、神経分化を制御するタンパク質「REST/NRSF」が関与し、加齢した父親の精子の非遺伝的要因が子どもに影響することを発見したと発表した。
同成果は、同大学大学院 医学系研究科・発生発達神経科学分野の大隅典子教授、東北大 加齢医学研究所 医用細胞資源センターの松居靖久教授、東京農業大学 応用生物科学部 バイオサイエンス学科 動物発生工学研究室の河野友宏教授、愛知県医療療育総合センター 発達障害研究所 障害モデル研究部の吉崎嘉一研究員らの共同研究チームによるもの。詳細は、「EMBO Reports」にオンライン掲載された。
将来の健康や特定の疾患へのかかりやすさなどは、胎児期や生後早期の環境に強く影響を受けると考えられている。これまでは、主に母体の栄養状態や薬物摂取など、母親側からの影響が注目されてきた。しかし近年になって、父親からの影響にも注目が集まりつつあるという。実際にヒトを対象とした疫学調査により、子どもの自閉症スペクトラム障害などの精神発達障害のリスクに関して、母親よりも父親の加齢が大きく関わることが世界各国で報告されるようになってきている。
加齢に伴い精子における「de novo突然変異」の蓄積および遺伝子発現を制御する「DNAメチル化」の異常が示唆されている。de novo突然変異とは両親兄弟には認められず、患者のみに認められる遺伝子変異のことで、親の生殖細胞形成の過程で生じることが多い。一方のDNAメチル化とは、DNAの特定の塩基が修飾(メチル基の付加)されることで、一般的には遺伝子のスイッチがオフになると考えられている。しかし現在までのところ、加齢に伴う精子のde novo突然変異の蓄積とDNAメチル化の異常の正確な分子メカニズムは不明だった。
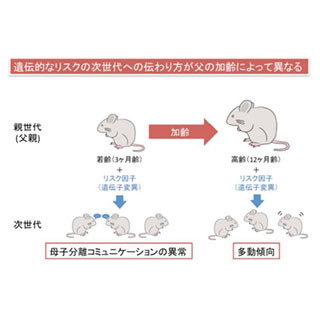
共同研究チームは今回の研究において、12か月齢以上(加齢)の父親マウスから生まれた仔マウスは、母仔間の音声コミュニケーションである超音波発声の頻度低下や鳴き方の単調化といった神経発達障害様行動異常を示すことを明らかにした。
-
父マウスの加齢に伴う精子のDNA低メチル化は仔マウスのコミュニケーション障害の原因となりうる。父マウスの加齢に伴う精子のDNA 低メチル化は仔マウスのコミュニケーション障害の原因となりうる (出所:東北大プレスリリースPDF)
次に、加齢マウスの精子を用いた全ゲノム網羅的メチル化解析が実施され、その結果として96か所のDNA低メチル化領域が同定された。さらに、このDNAメチル化領域の配列も解析された。すると、神経分化を制御することが知られるタンパク質のREST/NRSF(レスト/エヌアールエスエフ)の結合配列が、高頻度に存在することが発見された。
-
加齢父マウスの精子の低メチル化および加齢父由来仔マウス胎仔脳発現遺伝子制御において、REST/NRSFは共通分子基盤として機能する。全ゲノム網羅的メチル化解析により、加齢マウスの精子ゲノムには高頻度にDNA低メチル化領域が検出され、その多くに神経分化制御因子REST/NRSF 結合モチーフが含まれることが見出された (出所:東北大プレスリリースPDF)
続いて、神経発生が盛んになる胎生期の脳における網羅的遺伝子発現解析が実施され、その結果、加齢父マウス由来の胎仔脳では、自閉症関連遺伝子群の活性が強く、神経発生後期に発現すべき遺伝子群が前倒しで働いていることが発見された。加齢父マウス由来の胎仔脳では、REST/NRSFの標的遺伝子が高発現していることも見出された。
さらに、精子のDNA低メチル化が仔マウスに影響する可能性について検証するため、薬剤投与により若齢父マウスにDNA低メチル化を誘導し、生まれた仔マウスを解析。すると、超音波発声の頻度が低下し、鳴き方のパターンも単調化することが再現されたのである。
以上より、父マウスの加齢による仔マウスの行動異常には精子のDNA低メチル化が関与しており、その分子メカニズムとして、REST/NRSFを介した神経発生異常による可能性が示唆されたとした。
-
父親マウスの高齢化に伴う精子のDNA低メチル化は仔マウスの発達障害様行動異常の原因であり、その分子メカニズムとして、精子および仔マウス神経発生の共通分子基盤としてREST/NRSFが関与することが、今回の研究により、見出された (出所:東北大プレスリリースPDF)
今回の研究では、父親の加齢による子どもの神経発達障害の分子メカニズムについて、精子のDNAの低メチル化が関与することが見出された。このことより、今後、加齢によるDNAの低メチル化やその次世代への影響を防ぐことにより、神経発達障害の予防や治療法の開発が進むことが期待されるとした。