順天堂大学は、生理活性脂質12-HHTとその受容体BLT2を介した角膜上皮損傷の修復メカニズムの解明に成功したと発表した。
同研究は、順天堂大学大学院医学研究科生化学・細胞機能制御学の横溝岳彦教授、眼科学の岩本怜助教、松田彰准教授らの研究グループによるもので、同研究成果は、10月16日の英科学雑誌「Scientific Reports」電子版に掲載された。
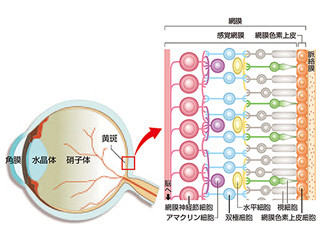
角膜は、眼のバリアとして機能しているが、コンタクトレンズや外傷などによって角膜上皮障害が生じることがある。また、非ステロイド性消炎鎮痛剤(NSAIDs)を含む点眼薬は白内障手術の術後などに頻用されているが、副作用として角膜上皮びらんや重症例では角膜穿孔を生ずることが問題となっている。
同研究グループは、過去に、腸管上皮細胞や皮膚ケラチノサイトに発現する新規のGタンパク質共役型受容体BLT2を発見し、BLT2を活性化する生体内リガンドの探索を行った結果、12-HHTと呼ばれる脂肪酸を同定した。その後、BLT2が皮膚ケラチノサイトに発現し皮膚の創傷治癒を促進するとともに、皮膚のバリア機能維持に必須であることを明らかにした。そこで、BLT2の皮膚の創傷治癒の促進作用が眼の角膜上皮障害にも有用ではないかという考えのもと、NSAIDs点眼薬の副作用の角膜上皮障害の実態と、その修復における12-HHT/BLT2の役割を明らかにする研究が行われた。
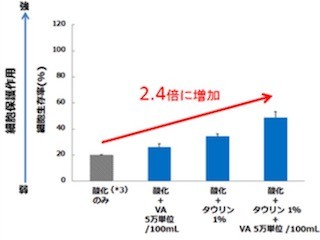
まず、マウスの角膜におけるBLT2の発現を調べたところ、BLT2が皮膚に匹敵する高いレベルで角膜組織に発現していること、そのリガンドである12-HHTが豊富に眼に存在していることが確認された。また、角膜上皮を直径2mmにわたって剥離し、経時的に損傷上皮の面積を計測するという角膜損傷修復モデルを作製したところ、NSAIDsであるジクロフェナクを含む点眼薬を投与すると角膜上皮損傷の修復が遅延し、BLT2を活性化する12-HHTや合成BLT2作動薬を点眼すると修復が促進することが発見された。
BLT2欠損マウスの角膜上皮損傷修復は、野生型マウスと比較して大きく遅延しており、ジクロフェナク点眼による更なる遅延は観察されなかった。以上の結果から、NSAIDsによる角膜上皮損傷修復の遅延は、プロスタグランジンの産生阻害ではなく、12-HHTの産生阻害という新しいメカニズムで生じていること、BLT2作動薬が角膜上皮損傷の新規治療薬となる可能性があることが明らかとなった。
現在、角膜外傷やコンタクトレンズ使用者、糖尿病で生じる角膜潰瘍に対する治療薬についてはアンメットニーズがあるが、同研究により今後、合成BLT2作動薬が角膜潰瘍の新規治療薬として臨床応用されることが期待されるということだ。