京都大学(京大)は9月29日、キネシンモータタンパク質と細胞骨格である微小管からなる「分子機械」を、微小流体デバイスと合わせて設計することで、目的地に狙い通りの微小管がたどり着くナノシステムを開発したと発表した。
同成果は、京都大学大学院工学研究科の横川隆司准教授、磯崎直人特定研究員らの研究グループと、マサチューセッツ大学アマースト校物理学科のJennifer L. Ross准教授、ウィスコンシン大学ラクロス校物理学科のTaviare L. Hawkins 准教授との共同研究によるもの。詳細は米国の科学雑誌「Science Robotics」に掲載された。
細胞内では、四方八方に張り巡らされたレールとしての微小管の上をキネシンが運動することで、細胞分裂や細胞内物質輸送などを実現している。このキネシンと微小管の組み合わせを1つの「分子機械」とみなし、その駆動力を用いて対象の分子を輸送するナノシステムの開発が行われてきた。
これまで、キネシンを基板に固定し、相対的に「分子シャトル」としての微小管を運動させる方法が提案されてきたが、その運動方向を思い通りに制御することは難しく、ナノシステムとして利用することは困難であった。
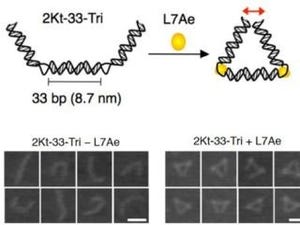
今回の研究では、微小管の電気的特性(電荷)および機械的特性(硬さ)を改変することで運動方向を制御し、3種類の微小管(硬い微小管、軟らかい微小管、電荷が大きく軟らかい微小管)をそれぞれ異なる場所へ輸送できることを示した。また、その運動にあわせて微小流体デバイスを設計し、微小管を電荷と硬さの差に応じて 80%以上の精度で分離することに成功したとしている。これにより、「分子機械」と微小流体デバイスの融合によるナノシステムの設計法を提案した。
今回の成果を受けて研究グループは、今後の展開について、がんマーカなどの輸送対象となる分子を微小管に結合させることで、複数の分子が同時かつ自律的に分離されるシステムを実現できるとコメント。また、同成果は、多機能な分子操作デバイスの開発につながるものであり、バイオ・医療・環境・化学などさまざまな分野の発展に貢献するものだとしている。