東京大学は、同大学医科学研究所の清野宏教授、大阪大学微生物病研究所の佐藤慎太郎特任准教授らの研究グループが、腸の表面などの粘膜面から異物(抗原)を取り込む能力を有するM細胞で、その機能に直接関わるタンパク質として「Allograft inflammatory factor 1(Aif1)」を同定したことを発表した。この研究成果は2月22日、英国科学雑誌「Nature Communications」オンライン版に掲載された。
粘膜を覆う上皮細胞の一種であるM細胞は、周辺の他の上皮細胞に比べて短くて疎な微絨毛を持っているうえ、粘液を産生しないことから、管腔側の外来抗原が落とし穴に入るように取り込まれやすい。加えて、色々な微生物に対する受容体を管腔側表面に発現しており、それらの効率的な取り込みに寄与していることが報告されている。しかし、抗原を運び込むトランスサイトーシスという機能に直接関わる分子群は、これまで報告されていなかった。
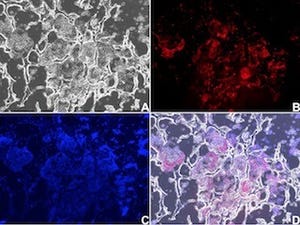
M細胞のトランスサイトーシスに直接関与する分子群を同定する目的で当研究グループは、M 細胞のほとんどを欠失するSpi-B欠損マウスとそのコントロールマウスから FAE を調整し、それらの遺伝子発現を解析・比較し、その中の候補遺伝子の一つとしてAif1を同定した。リアルタイムPCRにより、Aif1の発現が腸管上皮細胞系列ではFAEに特異的であり、かつ Spi-Bに依存していることが確認できたという。この結果がタンパク質レベルでも確認できたことから、Aif1は腸管上皮細胞系列においては M 細胞特異的発現分子である事が明らかになった。
次に、Aif1の成体内での機能を詳しく解析するため、Aif1を欠損するマウス(Aif1 KO マウス)を作製。このマウスでは、M細胞の発達・分化に影響はなかったが、人工粒子や腸内共生細菌、病原性細菌のエルシニア・エンテロコリティカの取り込みが顕著に減弱しており、 同分子がM細胞の機能に関わっている事が強く示唆されたという。
また、血球系ではAif1を欠損しないように、Aif1 KOマウスに野生型の骨髄を移植して同様の解析を行った結果、野生型マウスはAif1 KOマウス由来の骨髄を移植されても変わらずに物質の取り込んでいたが、逆にAif1 KOマウスは野生型由来の骨髄を移植しても物質の取り込みが改善することはなかったという。これらの結果は、抗原の取り込みにはM細胞中でAif1が発現し機能することが重要で、樹状細胞などの血球系細胞の影響はほとんどないことを意味するものだということだ。
今回の研究成果により、機能性分子であるAif1は、細胞の運動に関与するアクチンの動きを制御することで、外来抗原取り込み時に管腔側での細胞膜を変化させていることが示唆された。
一過性に Aif1の発現や機能をコントロールできれば、粘膜型ワクチンの抗原取り込み効率を上げることや、逆に病原性微生物の侵入を阻止し感染予防を可能にできる考えられるという。すなわち、注射型ワクチンに代わって、口や鼻から投与して粘膜に取り込む粘膜型ワクチンに役立つと期待されるということだ。
その一方で、 Aif1以外のM細胞機能関連分子群の存在を示唆する結果も得ており、このことから抗原取り込み能に寄与する分子が複数存在することが予想されるとしている。
研究グループは、今後もM細胞特異的に発現する分子を同定し、その機能を検証する事で、M細胞による抗原取り込み能の全容を解明する必要があると考えていると説明している。