量子科学技術研究開発機構(量研機構)は4月26日、多機能のナノ薬剤送達治療システムを開発し、薬剤の放出をMRIで高精度に観察するとともに、重粒子線治療との併用により治療効果が向上することをモデルマウスで確認したと発表した。
同成果は、量研機構放射線医学総合研究所 青木伊知男チームリーダー、國領大介研究員(現・神戸大学)、大阪府立大学 河野健司教授、弓場英司助教らの研究グループによるもので、4月20日付の国際科学誌「Translational Research」に掲載された。
ナノ薬剤送達治療とは、抗がん剤治療の副作用を軽減し治療効果を向上させる目的で、高分子の生体適合性材料であるポリマーやリポソームなどで作ったナノサイズの粒子に薬剤を封入し、患部に集中させるというもの。
しかし、がんの種類や状態によって治療効果に大きな差があることが知られている。その原因のひとつとして、ナノ粒子ががん全体に行き渡っていない可能性が示唆されている。そこで、薬剤のほかにMRI造影剤などをナノ粒子に封入することで、がんを診ながら治療を行う「セラノスティクス」と呼ばれる次世代の高精度医療が注目されている。
そこで今回、同研究グループは、がんに集まり、がんを診ることができ、がんを治療することができる、多機能のがん造影・治療リポソームを用いたナノ薬剤送達治療システムの開発を目指した。
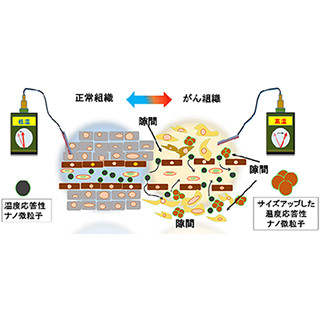
具体的には、まず脂質二重膜からなるリポソームの内部に抗がん剤と造影剤を封入し、粒子表面にはがんに集積する能力を高めるポリエチレングリコールと、41℃以上になると性質が変化する温度応答性ポリマーの2種類のポリマーを付加。このリポソームを血中に投与すると腫瘍に集まる様子がMRIで観察された。その後、患部を加温することで薬剤が腫瘍部分で放出される様子がMRIによってリアルタイムに観察されたという。
|
|
41℃以上に加温すると、温度応答性ポリマーが変形し、リポソーム内部からMRI造影剤と抗がん剤が放出される。放出されたMRI造影剤は、最も信号が高くなる濃度に希釈され、高信号を呈する (出所:量研機構Webサイト) |
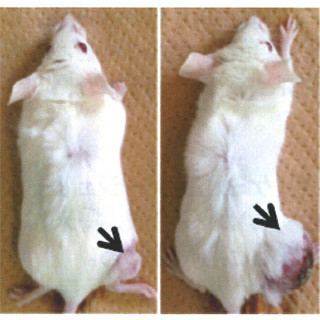
さらに同研究グループは、このナノ薬剤送達治療システムを、重粒子線治療を行った大腸がん移植モデルマウスに適用した結果、重粒子線単独の治療よりも、重粒子線治療とナノ薬剤送達治療システムを併用した場合のほうが、高い治療効果が得られることを確認している。
|
|
腫瘍部分により多くのリポソームが集まっていることがMRIにより観察できる(上)。重粒子線治療とナノ薬剤送達治療システムを併用した場合では、重粒子線治療単独に比べて、腫瘍体積がより縮小した(下) (出所:量研機構Webサイト) |
重粒子線がん治療では、転移したがんは適用外となるほか、転移リスクを下げるための抗がん剤併用治療も多い。同研究グループは今回の成果について、患者の負担をより軽減させる、効果的ながん治療の実現を目指す重要な一歩であると説明している。