京都大学(京大)は3月17日、ヒトES/iPS細胞から機能的な組織を作製するプロセス開発に向け、多種類の細胞環境を集積したデバイスを開発したことを発表した。
同成果は、京都大学物質-細胞統合システム拠点(iCeMS)の陳勇 特定拠点教授、同 亀井謙一郎 特定准教授、東京工業大学の眞下泰正 助教らによるもの。詳細は独科学誌「Small」に掲載された。
再生医療や創薬分野での活用が期待されるES細胞やiPS細胞などのヒト多能性幹細胞だが、目的の組織細胞や機能を獲得するためには、まだまだ課題が多く残されているという。
そうした課題の1つが細胞培養フラスコやティッシュなどを用いた従来型の細胞培養法だという。こうした方法は実験者にとって操作しやすいことがポイントだが、細胞からすると、本来、その機能を発揮するのに適した環境「細胞外環境」ではないため、必ずしも培養に適した環境とはいえなかったという。しかし、細胞外環境を構築するためには、ガス分子や成長因子、細胞外マトリックス(ECM)、硬さ・圧力などのさまざまな構成因子を組み合わせる必要があるが、目的とする細胞・組織を作るには、どのような組み合わせが適切なのかを試験で確かめる必要があるものの、従来の細胞培養法では、この細胞外環境を創出することが困難であり、そのため応用するための知見も不足していたという。
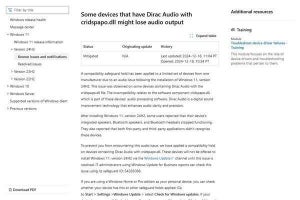
今回、研究チームはそうした状況の打破を目指し、生体内に近い環境を作り出すことが可能な「マイクロ流体デバイス」と「ナノファイバー」に着目。それぞれの技術と利点を融合させたハイブリッドデバイス「MACMEアレイ(Multiplex Artificial Cellular MicroEnvironment array:複合的な人工細胞外微小環境の群列)」を開発したという。
|
|
|
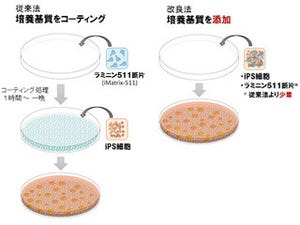
今回の研究で開発されたマイクロ流体デバイスとナノファイバーのハイブリットデバイス「MACMEアレイ」。それぞれの技術の利点を融合することで、細胞外環境の多様性を1つのデバイス内に創出することに成功したという (出所:京大Webサイト) |
具体的には、48個の微小な細胞培養チャンバを同デバイスに設置し、マイクロ流路による細胞の空間・密度制御機構とナノファイバーによる材料や密度などの異なる細胞足場を組み合わせて搭載したことで、多様性のある細胞外環境を1つのデバイス内に作り出すことを可能としたとしている。
|
|
|
|
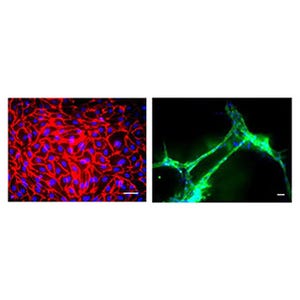
MACMEアレイのイメージ(左)と実物写真(右)。右の中央の写真は1つの細胞培養チャンバの画像。1つのアレイに付き、48個のマイクロ流路(細胞培養チャンバ)が設置されている。プレートのサイズは、通常の細胞培養実験に一般的に用いられる96ウェルと同じ設計となっている (出所:京大Webサイト) |
|
また、同デバイスは、96ウェルプレートに準拠したデザインとなっているため、特別な機械や技術などを準備・習得することなく、実験を行うことが可能だという。
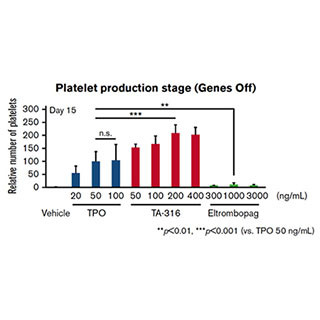
さらに研究チームでは、多様な細胞環境の中から目的の細胞機能を発揮することができるものを見つけ出す方法も開発。実際に、ヒトES細胞が未分化を維持したまま増殖するために最も適した細胞外環境を同定することに成功したとする。
なお研究チームでは、同デバイスについて、創薬にも応用可能としており、より正確な薬効評価や薬剤の安全性評価を行うことが可能となり、コストの削減などにもつながることが期待されるとするほか、細胞外微小環境はがん幹細胞においても重要であるとしており、今回の研究で開発された培養法を活用することで、新たな抗がん剤の開発にもつながることが期待されるとコメントしている。