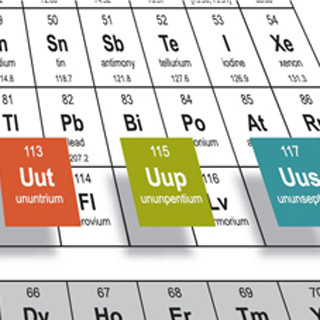
ヘリウム、ネオン、アルゴンなど、元素周期表の右端に並んでいる元素は、他の物質との反応性が低い「希ガス」として知られている。周期表のこの位置にある元素(第18族元素)は、原子のいちばん外側の電子軌道に収容できる最大数の電子が入った構造になっているため、他の原子とのあいだで軌道を共有して化学結合することができないためである。
希ガスを他の物質と反応させて希ガス化合物をつくるには、ほとんどの場合、極端な温度圧力下に置くなど特殊な条件が必要になる。とくにヘリウムは、希ガスの中でも化学的活性が最も低く、これまで安定したヘリウム化合物が生成された例はなかった。
米国、ロシア、中国、欧州の国際研究チームはこのほど、ヘリウムを超高圧条件下に置くことで、ヘリウムとナトリウムの化合物Na2Heが安定的に存在できることを発見したと報告した。また、Na2Heと似た構造の化合物Na2HeOが存在する可能性があることも理論的に予測した。研究論文は、化学分野の国際学術誌「Nature Chemistry」に掲載された。
研究チームは、超高圧下でヘリウム化合物Na2Heが存在できると予想。米国カーネギー研究所の高圧実験装置ダイヤモンドアンビルセル(DAC)を使って、実験的にこれを確認することに成功した。Na2Heが存在できる圧力は、113GPa(大気圧の約110万倍)超という超高圧であるという。
超高圧下での結晶構造解析には、第一原理計算にもとづく化学組成予測アプリケーション「USPEX」を使用した。
それによると、Na2Heは、画像のような「蛍石型」と呼ばれる結晶構造をもつ。ヘリウム原子は画像の緑色の立方体で表された位置にあり、立方体の8つの頂点部分にそれぞれ紫色の球で表されたナトリウム原子が入る。立方体間の隙間(ヘリウムが配位しない部分)には、電子対が局在化した状態で入る。ヘリウム原子とナトリウム原子は実際には結合していないが、ヘリウムの存在によってナトリウム同士の化学相互作用が変化し、電子対の局在化が起こることで、化合物の構造が安定して存在できるようになると考えられている。
Na2Heの結晶には、プラスの電荷をもつナトリウムイオンとマイナスの電荷をもつ副格子(電子対)の結合があることから、「エレクトライド」と呼ばれるイオン性化合物であるといえる。電子対が局在化している、つまり物質中を電子が自由に動くことができないため、Na2Heは電気の伝わらない絶縁体の性質をもつ。
もうひとつのヘリウム化合物であるNa2HeOも、15~110GPa程度の超高圧下で存在すると予想されている。こちらもイオン性化合物だが、Na2Heにおいて電子対が入っていた位置には、酸素イオンO2-が入る構造になる。
ヘリウムは、宇宙全体で水素についで大量に存在している元素である。超高圧下でのヘリウムの性質・挙動を解明できれば、木星型巨大惑星の内部や太陽などの極端条件下での化学反応プロセスについての研究が進展すると期待される。