京都大学(京大)などは12月26日、膜タンパク質「バクテリオロドプシン」が働く瞬間を原子レベルでコマ送り動画のように捉えることに成功したと発表した。
同成果は、京都大学大学院医学研究科 南後恵理子 客員研究員、岩田想 教授、ヨーテボリ大学 Richard Neutze教授らの研究グループによるもので、12月23日付けの米国科学誌「Science」に掲載された。
タンパク質は生命において重要な役割を果たす。タンパク質が働く仕組みには立体構造が深く関わっており、構造や仕組みを原子レベルで解明するために、これまで大型放射光施設「SPring-8」などでの放射光を利用したX線結晶構造解析が用いられてきた。しかし、従来のX線結晶構造解析ではタンパク質が動いている状態の観測は困難であるうえ、測定中の放射線損傷によりタンパク質の動きに影響を及ぼしてしまうという課題があった。
今回、同研究グループは、X線自由電子レーザー(XFEL)施設「SACLA」の高品質な光を用いた、連続フェムト秒結晶構造解析(SFX)法とポンプ・プローブ法を組み合わせた実験装置を開発。タンパク質の働きを開始するための可視光レーザーを導入し、空間的・時間的に高い精度で連続的に吐出されるタンパク質微小結晶へのXFELと可視光レーザーの照射が可能となった。
|
|
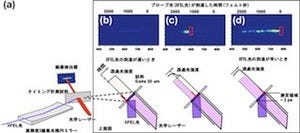
タンパク質の構造変化を捉える実験方法の概略図。微小結晶をXFEL照射領域に連続的に送り、可視光レーザーを照射して、光によるタンパク質の反応を開始させる。光照射後、ナノ秒からミリ秒後に起こるタンパク質の変化をXFELによる回折像を得ることによって調べる |
これにより、同研究グループは、高度好塩菌の膜に存在する「バクテリオロドプシン」という膜タンパク質の構造変化を捉えることに成功した。
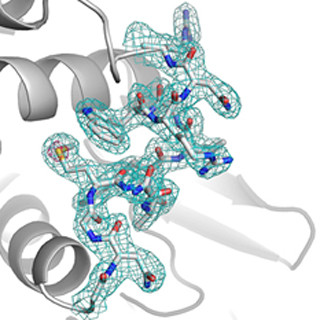
バクテリオロドプシンは、可視光や紫外光を吸収するレチナールを含んでおり、レチナールが光を受けると、その構造が変化し、細胞内の水素イオンを細胞外へ能動的に輸送するポンプとして機能する。
この水素イオン輸送の仕組みは長年未解明のままであったが、今回の実験ではタンパク質が光を受けた後、ナノ秒からミリ秒にかけて13の時点で測定を行い、コマ送り撮影のようにタンパク質の構造変化を観察。中間体構造を空間分解能72.1Åで決定することに成功し、レチナールが光を受けて構造変化する動きに伴い、周辺残基が細胞内側の方向に動くことが明らかになった。
同研究グループは、今回の成果について、将来的には医薬品や機能性分子の設計開発など、医療や工業への幅広い応用も期待されると説明している。