群馬大学(群馬大)は11月24日、熊本大学と理化学研究所およびトランスジェニックとの共同研究により、ホタルの発光機構と炎症反応を組み合わせ、炎症が生じた部分を明るく光らせることのできる遺伝子組換えマウスの作製に成功したと発表した。
同成果は、群馬大学大学院医学系研究科 岩脇隆夫 講師らの研究グループによるもので、11月24日付けの英科学誌「Scientific Reports」電子版に掲載された。
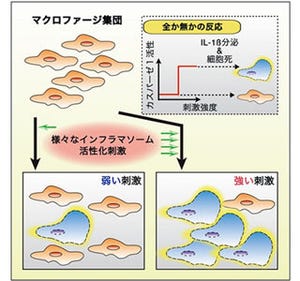
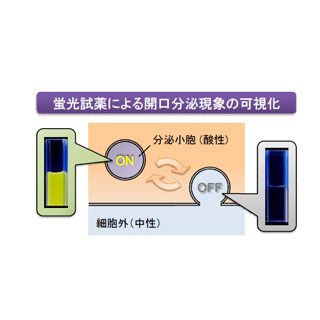
炎症反応のメカニズムは不明な部分も多いが、大抵の場合は細胞の傷害や菌・ウイルスの感染を免疫系細胞が感知し、炎症性サイトカインと呼ばれるタンパク質が産生・分泌されることにより起こる。炎症性サイトカインのひとつである「インターロイキン-1β」は、その成熟型が細胞外へ分泌されて炎症反応を引き起こすが、その産生・分泌を調節する仕組みは特徴的で、プロモーターに依存する転写活性化、「インフラマソーム」と呼ばれる酵素複合体を通じたタンパク質切断という2段階の生体反応を必要とする。
同研究グループは、生物発光反応を触媒する酵素「ルシフェラーゼ」の遺伝子にインターロイキン-1β遺伝子と分解シグナル遺伝子を順に連結し、それをインターロイキン-1βのプロモーター制御下においた人工遺伝子を作成した。
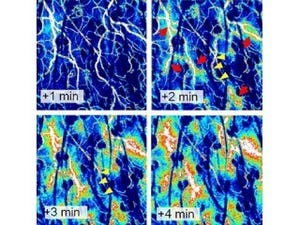
同人工遺伝子を持つマウスにおいて、炎症が起きるような状況ではプロモーターが活性化するため、制御下にあるルシフェラーゼ遺伝子の転写が促進される。その後、翻訳されるルシフェラーゼタンパク質はインターロイキン-1βタンパク質に作用するインフラマソームのために連結されていた分解シグナルから切り離され、安定的に維持され発光する。逆に炎症がない状況下では、プロモーターが活性化しないので、ルシフェラーゼ遺伝子の転写も促進されない。つまり、炎症が生じた身体の部分を炎症が生じたときにだけ明るく光らせることができる。
これまでにもインターロイキン-1βの性質を利用した炎症可視化技術はほかの研究グループによっていくつか開発されてきたが、このマウスは性能面でそれらに勝っているという。今後、同マウスからの発光シグナル観察を通して、疾患や外傷などに伴う炎症の状態や抗炎症薬による効果などが今まで以上に容易かつ正確に調べられるようになることが期待される。