京都大学は6月22日、大腸炎に伴い大腸がんを発症するマウスモデルを用いて、腸がん形成進展を促進する大腸での炎症反応がPGE2-EP2経路によって制御されることと、EP2を阻害することが大腸がんの治療につながることを解明したと発表した。
同成果は京都大学 大学院医学研究科・次世代免疫制御を目指す創薬医学融合拠点(AKプロジェクト)の青木友浩 特定准教授、成宮 周 特任教授らの研究グループによるもので、米国学会誌「Cancer Research」に掲載された。
大腸がんの発生・進展には炎症が関係しており、アスピリンなどの非ステロイド性抗炎症薬(NSAIDs)がリスクを低下させることが知られている。しかし、NSAIDsには副作用があり投与に慎重を要するほか、代替として開発されたCOX-2阻害薬も心血管障害の副作用があるため使用には制限がある。
NSAIDsとCOX-2阻害薬はいずれも生理活性脂質である一連のプロスタグランジン(PG)の合成を阻害して効果を発揮する。これはPG経路が大腸がんの発生・進展に関与していることを示しているが、その機序については詳しくわかっていなかった。
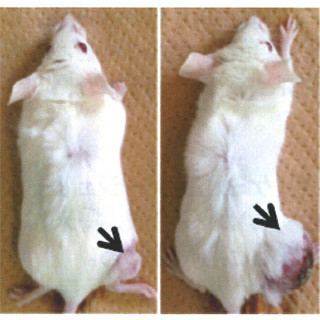
同研究グループは今回、大腸炎に伴い大腸がんを発症するモデルマウスを用いて、炎症性大腸がんの形成に寄与するPG受容体として、PGの一種であるPGE2の受容体の1つEP2を同定。続いて、がん組織内のEP2発現細胞を検討したところ、腸組織内に浸潤する主要な炎症細胞である好中球と、腫瘍細胞を取り囲むように存在している線維芽細胞(腫瘍関連線維芽細胞)がEP2を発現しており、この2つの細胞種でPGE2-EP2経路が周囲の細胞に刺激を与えるさまざまなタンパク質や細胞の増殖を助ける成長因子の発現を増加させることで大腸がん形成を促進すること、これらの細胞は自らPGを産生してこの経路をさらに増幅していることを突き止めた。また、選択的EP2阻害薬を投与することで、大腸での炎症とがん形成を抑制できることを確認した。
今回の研究で大腸がんの促進に働くPGの種類とその作用機構が明らかになったことで、現在使用されているNSAIDsやCOX-2阻害薬を超えた、副作用の少なく、より安全な新規の大腸がんの予防・進展抑制薬の開発につながることが期待される。