京都大学iPS細胞研究所(京大CiRA)は、遺伝子の運び屋であるベクターの一種である、「ピギーバックベクター」を用いて血液凝固因子の遺伝子全長を導入し、血友病Aモデルマウスの血液凝固機能を改善することに成功したと発表した。
この成果は、同研究所の堀田秋津 助教授と奈良県立医科大学の松井秀人 講師らの研究グループによるもので、米科学誌「PLOS ONE」に掲載された。
血友病は血を固めるためのタンパク質が生まれつき少ない、あるいは無いために、血が止まりにくくなってしまう病気。そのうち、血友病Aは血液凝固第VIII因子をつくるFVIII遺伝子の変異により、第VIII因子が欠損して起こる遺伝子疾患とされる。主な治療法としては欠乏している第VIII因子タンパク質製剤の投与があるが、短期間で活性が消失するため、重度の患者には繰り返し投与することが必要となる。この問題に対し、長期間安定的にFVIII遺伝子を発現し第VIII因子を分泌させる遺伝子治療が可能となれば、患者の生活の質を改善できると考えられている。
遺伝子治療分野においては、変異した遺伝子に替わる正常な遺伝子を外部より導入するために、導入効率の観点からウイルスベクターが主に使用されている。しかし、導入したウイルス由来タンパク質に対する免疫応答や、予期せぬウイルス配列の変異などのリスクがあるほか、FVIII遺伝子はサイズが大きすぎてウイルスでは運べないという問題があった。そのため、従来はFVIII遺伝子の一部を切り詰めた欠損型のFVIII遺伝子が主に使用されていた。
そこで同研究では、高い転移活性をもち、変異ウイルスの発生リスクやウイルスを抗原とする免疫応答を回避できると考えられているピギーバックベクターを、FVIII遺伝子の導入に用いることで、ウイルスベクターを用いずに全長型のFVIII遺伝子を導入することができるかどうかを検証したという。
まず、ピギーバックベクターにサイズの異なる様々な遺伝子を搭載し、ヒト腎臓由来培養細胞へ遺伝子導入を行ったところ、搭載する遺伝子のサイズは小さいほど導入効率が高く、ヒトの全長型のFVIII遺伝子を搭載すると、低い割合ながらも、欠損型のFVIII遺伝子と同程度に遺伝子導入できることが確認されたという。
次に、欠損型のFVIII遺伝子と、全長型のFVIII遺伝子をヒト腎臓由来培養細胞とヒトiPS細胞それぞれへ導入して、遺伝子発現および分泌FVIIIタンパク質の活性を測定。すると、欠損型に比べて全長型を導入した方が双方の細胞で遺伝子発現が高く、腎臓由来培養細胞ではFVIIIタンパク質の活性も高いことが観察されたという。
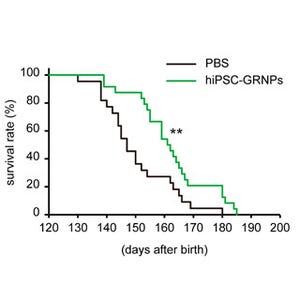
そして、全長型FVIII遺伝子を搭載したピギーバックベクターを、血友病Aモデルマウスに導入した結果、300日以上にわたって、活性を持ったFVIIIタンパク質が血中に分泌されていることが確認され、さらに、ピギーバックベクターの注入による遺伝子導入を4週間おきに3回行う事で、FVIIIタンパク質の分泌量を増強することができることも判明したという。
最後に、血友病Aモデルマウスのしっぽからの出血時間を測定したところ、ベクター注入が無いと平均18分程度出血が続いたが、ピギーバックベクター注入により遺伝子導入したマウスでは、平均6分ほどで止血し、血液凝固機能が回復していることが確認された。
同研究チームは、「今回の研究により、ピギーバックベクターを用いることで、全長型FVIII遺伝子を送り届けて安定的に発現させることができることが分かった。この方法は将来的に、血友病などの遺伝子治療に貢献できると考えられる」とコメントしている。