横浜市立大学(横浜市大)は3月5日、神経の伸長方向のコントロールに重要な役割をするタンパク質「セマフォリン3A」が、脳内で学習や記憶を司る役割を担う「グルタミン酸」と結合し、脳内の情報を伝達する「グルタミン酸受容体」の神経細胞の細胞体や樹状突起における場所を、神経突起の末端の遠隔からコントロールするというこれまで見つかっていなかった仕組みを発見したと発表した。
同成果は、同大学術院医学群の山下直也 助教、五嶋良郎 教授(薬理学教室)らによるもの。詳細は「Nature communications」に掲載された。
神経細胞は、「細胞体」、「樹状突起」、「軸索」の3つ部分から形成されており、通常、神経を介する情報の伝達は、その軸索の成長末端部にある成長円錐を介して、情報を伝える相手の細胞(標的細胞)に到達し、神経伝達の場であるシナプスを作る際、シナプスの形成が起こると同時に、樹状突起が複雑になるという現象が知られていた(「樹状突起」、「細胞体」、「軸索」の順序で伝搬していく)が、そのメカニズムは、完全には明らかにはされておらず、これまでは神経回路が形成される際に、神経栄養因子が神経の末端から取り込まれて細胞体に情報を伝えるということを通じて神経伝達が行われている神経を生存させ、使われていない神経を排除する仕組みが存在するとされてきた。
「セマフォリン3A」は、神経の突起先端に作用してその伸長を抑制する分子で、アトピー性皮膚炎の患者では皮膚内の量が低下して神経が伸長し、かゆみに対して敏感になることが知られている。
また、「グルタミン酸受容体」は、他の神経細胞から情報の入力を受ける最も重要な担い手であり、この分子が本来存在する樹状突起の部分で正常に分布して働かない場合、アルツハイマー病や統合失調症などの精神神経疾患のような病態が発症することが考えられている。
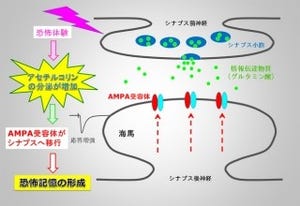
今回の研究では、セマフォリン3Aを海馬の培養神経細胞の軸索成長円錐に作用させた場合、セマフォリン3Aの受容体であるプレキシンA4という分子が、セマフォリン3Aとともに逆行性の軸索輸送に乗って、その作用点から遠く離れた細胞体や樹状突起に運ばれ、逆行性の軸索輸送を介して樹状突起のグルタミン酸受容体の存在する場所を適切にコントロールする仕組みが存在することが見出された。
また、その際、GluA2というグルタミン酸受容体を捕まえて樹状突起に運ぶという従来にない新しいメカニズムを使って、グルタミン酸受容体の樹状突起における場所をコントロールしていることも確認したほか、このグルタミン酸受容体の場所のコントロールが正常に行われない場合、樹状突起の成熟が正常に起こらないことも確認したという。
なお、研究グループでは、セマフォリン3Aは、神経栄養因子と同様に、標的細胞やその周辺の細胞から分泌されるため、今回の発見は、どのようなメカニズムで情報の出力系(シナプス前部)と情報の入力系(樹状突起)が同期して成熟するのか、といった長年の課題に答える神経生物学上の成果と説明しており、グルタミン酸受容体の働きの障害が原因と考えられるアルツハイマー病や統合失調症などの精神神経疾患の新たなメカニズムの解明に繋がる成果として、新たな治療法の開発につながることが期待されるとしている。