京都大学(京大)は10月14日、細胞内および細胞内小器官の温度計測を可能とする温度センサタンパク質を開発し、生体の恒常性を担う熱産生機構の可視化に成功したと発表した。
同成果は、同大の森泰生 地球環境学堂教授(工学研究科合成・生物化学専攻両任)、清中茂樹 同准教授らによるもの。詳細は2013年10月13日13時(米国時間)に、「Nature Methods」電子版に掲載された。
恒温動物の体内は、外気温の変化によらず常に37度付近に保たれており、従来の生物学では、すべての生命現象は生体(細胞)温度が37度付近であるという前提で研究されてきた。しかし、核やミトコンドリアをはじめとする細胞内小器官は、複雑な化学反応をともなう固有の機能を担っており、すべての細胞内小器官の温度が均一であるとは考えにくく、仮に細胞内温度に不均一性が存在するのであれば、温度の不均一性によって生体機能が制御されている可能性があると考えられるが、これまで有用な細胞内の温度計測法は存在していなかった。また、細胞内の局所で発生した熱はすぐに拡散してしまうため、細胞内の熱産生および温度分布を計測するためには、まさに熱が産生されている場所(細胞内小器官)で温度計測を行う必要があるという課題もあった。
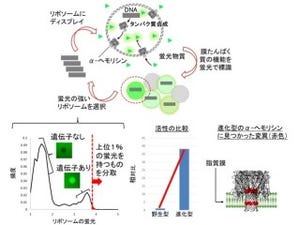
そこで今回研究グループは、遺伝子工学的な手法を用いて、細胞内および細胞内小器官の温度計測を可能とする温度センサタンパク質(thermosensor GFP:tsGFP)を開発した。tsGFPは、サルモネラ菌に存在する温度感知タンパク質で、単量体と2量体形成との遷移が37度付近で鋭敏かつ可逆的に起こる「TlpA」を緑色蛍光タンパク質(GFP)と適切に融合することで得たもので、TlpAを融合したtsGFPは、37度付近の温度変化を鋭敏に感知し、蛍光の変化を起こすこととなる。また、tsGFPは、遺伝子でコードされるために、非侵襲的に生細胞内・組織内に導入可能という特徴があり、細胞内小器官に標的できるシグナル配列を付与することで、各々の細胞内小器官における温度計測も可能になるという。
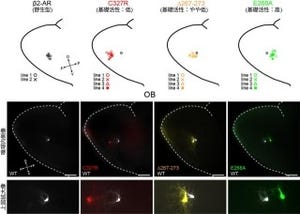
実験では、tsGFPを用いて熱産生組織として考えられていた褐色脂肪細胞からの熱産生の可視化に成功した。この結果、熱産生に関与していると考えられてきた褐色脂肪細胞では、ミトコンドリアに発現する温度センサ(tsGFP1-mito)を用いることで、褐色脂肪細胞内のミトコンドリアから熱産生が行われていることを直接的に観測することに成功したという。
また、小胞体に発現する温度センサ(tsGFP1-ER)を用いることで、非ふるえ熱としての寄与で意見が分かれていた筋細胞の小胞体からの熱産生の可視化にも成功し、筋細胞も熱産生を行うことを直接的に証明したという。
これらの熱産生細胞に関する研究結果について研究グループでは、肥満が問題となっている欧米を中心に、新たな肥満解消方法の標的として、熱産生を促す創薬の開発につながることが期待されると説明するほか、今回開発された温度センサが、細胞内のミトコンドリアに温度分布が存在すること、ならびにその温度分布がATP合成と関連していることを明らかにしたことから、細胞内の温度の不均一性が細胞内機能と関連する可能性が示唆されたとコメントしている。