東京工業大学(東工大)は9月25日、遺伝子発現を光で自在に調節する光依存型転写制御システム「ピッコロ(PICCORO:PixD complex-dependent control)」を開発し、ゼブラフィッシュの尻尾の形成を光のON/OFFで制御することに成功したと発表した。
成果は、東工大 バイオ研究基盤支援総合センター兼地球生命研究所の増田真二准教授、同・生命理工学研究科の田中幹子准教授らの研究チームによるもの。研究の詳細な内容は、9月24日付けで米化学会誌「ACS Chemical Biology」オンライン版に掲載された。
遺伝子発現は、生命現象の根幹をなす反応であり、その反応機構の解明と応用は、生命科学の中心的課題だ。具体的には、遺伝子の実体であるDNAからRNAが合成され、さらにRNAからタンパク質が作り出される一連の過程を指す。これまで、主に薬剤添加による遺伝子発現誘導システムが構築され、それらは多くの分野でなくてはならない実験手法として頻繁に用いられている。
しかし誘導した遺伝子発現をOFFにする技術や、局所的に発現を誘導できるシステムの構築が、特に、生物個体の体が作られる仕組みを明らかにする発生生物学の分野で望まれていたが、これまでのところ、実用化レベルには至っていない。
増田准教授らは、これまでの研究で光合成細菌「シアノバクテリア」から青色光受容体タンパク質「PixD」を発見しており、その機能解析を進めてきた。PixDは、別のタンパク質「PixE」と光依存的に相互作用することで、具体的には暗所で結合し、光を当てると離れることで、光シグナルを下流へ伝える機能を持っていたのである。
より具体的に説明すると、光受容体PixDは光の色と強さを認識し、その光シグナルをPixEに伝え、最終的にシアノバクテリアが光の方向へ移動する生理現象をコントロールするというわけだ。そこで増田准教授らは、この光受容体PixDの性質を利用すれば、光依存的に任意の転写因子の機能を制御できるのではないかと考え、以下の研究開発が進められたのである。
まず、光受容体PixDが結合するPixEの最小領域を決定するところからスタート。次に、PixDが結合するPixEの最小領域を、ゼブラフィッシュの尻尾の形成を制御する転写因子に融合させた。すると、その組換え転写因子は試験管内で光依存的にPixDと相互作用するようになったのである。
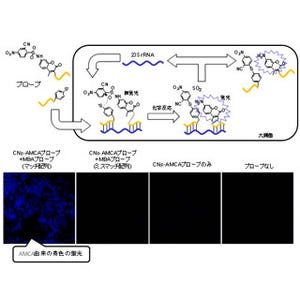
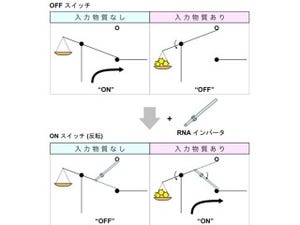
通常、転写因子は数個が集合した状態で機能する仕組みだ。そのため、PixDが転写因子に結合すると転写因子の集合体形成が阻害され、結果的に転写調節能を失うことが判明(画像)。すなわち、PixDが存在する条件下において、この転写因子はPixDと複合体を形成するため転写調節能を失い、光照射下ではPixDが外れ、再び転写調節能を回復すると考えられたのである。
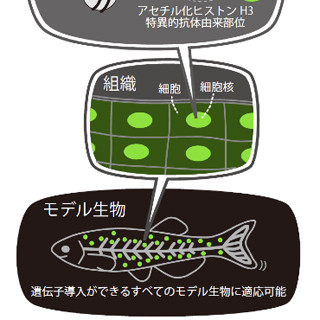
この現象を生体内で確認するため、増田准教授らは光受容体PixDを発現するゼブラフィッシュを作成し、その中で上記転写因子の機能が光で調節できるのかどうかを調べることにした。すると、尻尾の形成が光の有無で変化することが確認され、実際にこの系が生体内で働きうることが示されたのである。
原理的に、ピッコロ法はいかなる転写因子にも応用可能で、今後、さまざまな生命科学研究に用いられることが期待されるという。特に、タンパク質の相互作用により遺伝子発現誘導のスイッチングが可能なこの技術は、DNAやRNAを打ち込むことで達成させていた従来の方法と異なり、個体発生のいかなる段階でも遺伝子発現をON/OFFすることが可能だ。これにより、今まで解析が困難であった神経発生や代謝調節などに関わる遺伝子の解析が進むと期待されるとしている。