放射線医学総合研究所(NIRS)と科学技術振興機構(JST)は9月19日、脳内での神経細胞の骨格を形成する「微小管」に結合するタンパク質「タウ」の蓄積をPET(Positron Emission Tomography:陽電子断層撮影法)により画像化することに成功し、タウの蓄積とアルツハイマー病の重症度の関連性を示唆する成果を得たとし、さらにアルツハイマー病以外の認知症におけるタウの画像化においても有効であるとの成果を得ることができ、多様な認知症についての発症メカニズムの解明や、症状からの診断が困難である発症初期の診断、重症度の客観的な診断、認知症治療薬の開発促進が期待されると共同で発表した。
成果は、NIRS 分子イメージング研究センター 分子神経イメージング研究プログラム 脳分子動態チームの樋口真人チームリーダーらの研究チームによるもの。研究の詳細な内容は、日本時間9月19日付けで米科学誌「Neuron」オンライン版に掲載された。
厚生労働省の調査によると、国内の認知症患者は2012年の時点で約462万人にのぼることが判明している。この内、約半数はアルツハイマー病患者であるという。アルツハイマー病患者数はこの数年でも急増しているが、人口の高齢化が進むにつれて、今後ますます増加すると予想されているところだ。
アルツハイマー病患者の脳内には「アミロイドβ(Aβ)」とタウの2つのタンパク質が蓄積し(画像1)、これに伴って神経細胞が死んで脱落することから脳が萎縮することで(画像2)、物忘れなどの症状が発現してくるとされている。こうした異常タンパク質の蓄積は、存命している状態で検出することは難しく、これまで患者の他界後に脳を解剖して調べられていた。
近年、病的な蓄積をするタンパク質に特異的に結合する薬剤を開発し、これを用いることで生きている患者の脳における病変を画像化する研究が進められている。薬剤を特定の放射性同位元素で標識してこれを投与した患者のPET撮影を行い、薬剤から出てくる放射線のデータを解析することで、タンパク質の異常な蓄積を画像化することが可能になるという仕組みだ。
また最近の研究から、神経細胞死に密接に関わるのは神経の外に蓄積するAβではなく、神経の中に蓄積するタウであると考えられていることから、NIRSでは、タウ病変を画像化することでAβの画像化では十分評価できなかったアルツハイマー病の病勢評価や根本的治療法の開発が可能になると考察し、生体脳でタウ病変に結合するPET薬剤の開発に着手した次第だ。
タウ病変を画像化することを目的としたPET薬剤の開発には、世界的に数多くの研究チームが取り組んでいる。しかし、実際の脳組織や生体モデルを用いずに試験管内の反応性に基づいて薬剤を選び出しても、有望な薬剤は得られてこなかった。
そこでNIRSが採用したのが、脳組織スライスにさまざまな構造を持った薬剤を直接反応させることによって、脳内タウ病変に結合する薬剤を探索し、その結果からタウ凝集体の分子構造に至適な分子長があることを見出しすことで新たな化合物群を作製するという手法だ。その化合物群は、アルツハイマー病に限らず、これ以外の認知症やタウを過剰発現させた認知症モデルマウス(タウ病変モデルマウス)のタウ病変にも結合することが確かめられている。
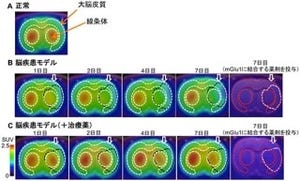
次に、化合物群の中でタウ病変に選択的に結合する薬剤3種類が選び出され、放射性同位元素である11C(質量11の炭素)で標識して、タウ病変モデルマウスに投与しPET撮影を実施。すると、薬剤「PBB3」の標識体「[11C]PBB3」が最も高いコントラストでタウ病変を検出できることが判明したというわけだ(画像3)。
画像3は、[11C]PBB3投与後の認知症モデルマウス脳PET画像。正常マウス(上段)では脳内の薬剤集積量はわずかだが、タウを過剰に発現させたモデルマウス(中段)では薬剤集積が見られ、特に脳幹と呼ばれる脳の深部領域(白矢印)で強い集積が認められた。このモデルマウスの脳をスキャン後に摘出してタウ病変の分布を蛍光色素で調べた結果(下段)、PBB3の強い集積が見られた脳幹に多数のタウ病変が見出された。従って、モデルマウスのPET画像はタウの蓄積を反映することがわかったのである。
基礎研究で[11C]PBB3の有用性が確かめられたことより、アルツハイマー病患者3名と、認知機能が正常な高齢者3名を対象とした探索的な臨床研究が実施された。この臨床研究では同一の被験者において、[11C]PBB3を投与した際のPET画像を、Aβ病変を画像化する「[11C]PIB(Pittsburgh Compound-B:ピッツバーグ化合物)」を投与した際のPET画像との比較が行われたのである。
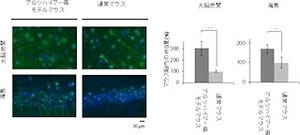
その結果、[11C]PBB3はアルツハイマー病患者脳の海馬という領域に強く集積したが、[11C]PIBは海馬以外の領域(大脳皮質など)に強く集積することが判明(画像4)。これまで多くのグループによる死後脳の研究で、アルツハイマー病患者の海馬ではタウ病変が大量に蓄積し、Aβ病変は大脳皮質ほど多くないことが明らかになっていることから、[11C]PBB3の海馬への集積はこの薬剤のタウ病変への結合を示す証拠と考えられるという。
画像4。臨床研究で得られたMRIおよびPET画像。同じ被験者で[11C]PBB3(タウ病変を検出)と[11C]PIB(Aβ病変を検出)の脳内集積が比較されたもの。アルツハイマー病患者(上段)では、正常高齢者(下段)に比べて海馬を含む領域(矢頭)で[11C]PBB3の集積が顕著に見られた。一方、[11C]PIBは海馬領域への集積はあまり見られず、Aβが多量に蓄積する大脳皮質で集積が認められた形だ。
海馬領域ではタウは高度に蓄積するが、Aβ蓄積は比較的少ないことより、[11C]PBB3の脳内集積はアルツハイマー病患者でもタウ蓄積を反映すると考えられるという。MRI画像では、アルツハイマー病患者の海馬領域における萎縮が顕著であり、タウ蓄積によって神経細胞死が起こったことが示唆されるとしている。
さらに[11C]PBB3の集積部位は、初期には海馬付近で認められ、アルツハイマー病を発症して重症化するに従い、大脳辺縁系全体、さらに、大脳皮質の広い領域へと拡大することがわかった(画像5)。この所見は、脳を解剖して調べることで推測されていたタウ病変部位拡大の推移とよく一致しているという。
これに対して、[11C]PIBの集積部位はアルツハイマー病の発症後は、極めて重度の場合を除き変化せず、疾患の重症度を反映してはいなかった。従って、[11C]PBB3を用いたPET検査により、タウ蓄積部位の広がりに基づいて、アルツハイマー病の発症や進行を客観的に評価することが可能になったのである。
画像5は、アルツハイマー病の発症と進行に伴うPET薬剤集積量の変化。[11C]PBB3の脳内集積は、海馬(矢頭)を含む領域で増加が始まり、アルツハイマー病の発症と進行に伴って広範な領域で増加をきたすことが明らかになった。これに対して、[11C]PIBの脳内集積はアルツハイマー病発症時には広い範囲で増加を認め、病気が進行しても、極めて重度の場合を除き集積量や分布にほとんど変化が見られていない。以上より、[11C]PBB3で検出されるタウ蓄積の量と分布は、アルツハイマー病の発症と進行に対する客観的な指標となることが示されたのである。
また、[11C]PBB3はアルツハイマー病以外の認知症で蓄積するタウ病変にも結合することが基礎研究で示唆されていたが、実際に非アルツハイマー型認知症の患者でもタウ蓄積を画像化することに成功した。「皮質基底核変性症」という、運動障害と認知機能障害を主症状とする疾患の患者に[11C]PBB3を投与してPETを実施したところ、大脳皮質に加えて、基底核、脳幹と呼ばれる脳の深部においても薬剤の顕著な集積が認められたのである(画像6)。これらの領域は皮質基底核変性症でタウが蓄積すると考えられている部位に一致していたという。
また、[11C]PIBはこの患者で集積が見られず、Aβは蓄積していないことが確かめられている。これらの結果に基づき、Aβ蓄積が起こらない非アルツハイマー型の認知症において、[11C]PBB3が鑑別診断に有力な手掛かりをもたらすことが明らかになったというわけだ。
画像6は、皮質基底核変性症(非アルツハイマー型認知症)の患者におけるPET画像。[11C]PBB3の脳内集積は、大脳皮質でも軽度上昇を認めたが、大脳基底核(矢頭)や脳幹(矢印)での集積増加が顕著であることが確かめられた。これらの領域は、皮質基底核変性症でタウが蓄積する脳部位と一致した形だ。[11C]PIBの脳内集積は見られず、Aβは蓄積していないと考えられるという。
今回の成果により、新しいPET薬剤PBB3を用いることで、アルツハイマー病の脳内のタウ蓄積を明瞭に画像化できるようになった。また、PBB3はアルツハイマー病だけでなく、ほかの認知症で形成されるタウ病変も描出し、神経細胞の脱落を鋭敏に検出できる手段として認知症診断に広く応用できる可能性も明らかになっている。
また、タウ病変は脳内の狭い領域から始まって広がっていくことがわかってきたことから、物忘れや感情の変化といった認知症の症状が脳内のどのような神経回路の異常で起こってくるのか、さらにどのような条件で症状の進展が止められるかといった研究に極めて重要な手掛かりを与えてくれるものと期待されるという。
さらに、タウ病変が神経細胞死を反映していることから、このような治療薬は認知症の症状が明確になった段階でもそれ以上の神経細胞死を防ぐことにより、認知症の症状の重症化を防ぎ、介護の負担を大幅に減少できる可能性があるとする。治療薬を臨床試験(治験)で評価する際に、モデルマウスとヒトで同じPET薬剤を利用できることから、治療薬開発の基礎と臨床を切れ目なくつなぐことが可能になる点も今回のポイントだ。認知症治療の切り札となりうる抗タウ療法の実現へ向けて、今回の研究の成果が大きく貢献することが期待されるとしている。
一方、近年米国ではアメリカンフットボールの選手や、戦争で頭に外傷を受けた軍人に精神障害が起こり、その死後、脳解析から外傷後の脳にタウの異常蓄積があることが注目されるようになってきた。今後は、認知症以外における外傷後の精神障害など、機序が明らかではなかった脳の機能障害の研究にもタウ病変イメージングが応用されていく可能性があるとしている。