宮崎大学は8月1日、理化学研究所(理研)との共同研究により、ヒト型iPS細胞をより質の高い「マウス型様iPS細胞」に変換し、目的細胞への「分化誘導効率」を向上させることに成功したと発表した。
成果は、宮崎大 テニュアトラック推進機構の本多新 TT准教授(理研 バイオリソースセンター(BBC) 客員研究員兼任)、理研BBC 遺伝工学基盤技術室の小倉淳郎 室長らの研究チームによるもの。研究は科学技術振興機構さきがけ「iPS細胞と生命機能」の一環として行われ、詳細な内容は米科学誌「The Journal of Biological Chemistry」印刷版10月号に掲載されるに先立ち、オンライン版に7月23日付けで掲載さた。
iPS細胞(人工多能性幹細胞)は、自分自身の細胞に山中ファクターとして有名な4つの外来遺伝子(OCT3/4、KLF4、SOX2、c-MYC)を導入するだけで樹立できることから、受精卵や胚を利用する必要がなく、また免疫拒絶も起こらないため、再生医療研究などへの展開が期待されているのは、多くの人が知るところだ。一方、胚から樹立されるES細胞(胚性幹細胞)は、倫理や拒絶の問題があるものの、質的には非常に優れていると考えられている。
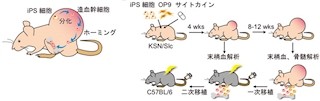
また、iPS/ES細胞などの多能性幹細胞には、マウスやラットから樹立され、キメラとして個体に寄与することが可能な上に生殖細胞などにも分化できる質の高い「マウス型」と、多くの組織に分化可能ではあるものの、その分化能力に制限がある「ヒト型」という2つのタイプに分けられることが知られていた(画像1)。
ヒトを含む多くの動物から樹立されるiPS/ES細胞は、そのほとんどがヒト型であり、マウスとラットなど限られた小動物でのみマウス型の多能性幹細胞を樹立することが可能だ。そのため、現在世界中で盛んに行われているのが、ヒト型のiPS細胞をマウス型に変換する技術の開発である。そのため、多能性幹細胞は分化誘導した後にさまざまな研究に利用されることが多いため、マウス型に変換したiPS細胞の質が本当に高まっているのか否かについて、分化能力に焦点を当てて調べるような研究が求められていた。
そこで研究チームは、ヒト型多能性幹細胞であるウサギES細胞、成体ウサギ肝臓由来iPS細胞、および成体ウサギ胃由来iPS細胞には遺伝子発現相違があることから、その相違が実際に体外で目的の細胞に分化誘導した場合に、影響を及ぼすのか否かの検討を実施した。
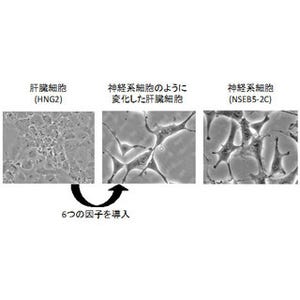
その結果、iPS細胞を神経系細胞(神経幹細胞、神経繊維、アストロサイト)に分化誘導したところ、肝臓から樹立されたiPS細胞や樹立初期のiPS細胞はES細胞に比べて、その効率が低い場合があることが判明。しかし、一定期間以上培養し、幹細胞として安定させれば、肝臓由来のiPS細胞でもES細胞と同じように分化誘導できることが明らかになったのである。
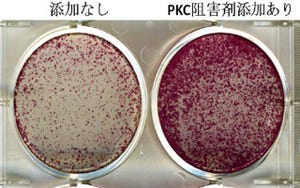
次に、より分化誘導が困難な神経系細胞の「オリゴデンドロサイト」について、ES細胞とiPS細胞を用いた比較を実施。その結果、iPS細胞はそのドナー細胞差や培養期間の長短に関わらず、ES細胞よりも分化効率が低いことがわかった(画像2~4)。
|
|
|
|
|
ヒト型ES/iPS細胞をオリゴデンドロサイトに分化誘導した際の相違。ES細胞をオリゴデンドロサイトに分化させた場合に比べて、iPS細胞ではその効率が低いことが判明。分化誘導したオリゴデンドロサイト(赤・黄)のiPS細胞(画像2(左))、ES細胞(画像3(中))、iPS細胞とES細胞の比較分布効率(画像4(右)) |
||
続いて研究チームは、ヒト型であるウサギiPS細胞をマウス型に変換することができれば、ES細胞よりも低いiPS細胞の分化能力を改善することができるのではないかと考察し、ウサギiPS細胞のマウス型化に挑んだ。山中ファクターの1つでもあるOCT3/4遺伝子を過剰に発現させて、さらに培養環境を変化させることにより、部分的にマウス型の特徴を示すウサギiPS細胞を樹立することに成功。「マウス型様(Naive-like)iPS細胞」と名付けられた。
そしてマウス型様に変換したiPS細胞をオリゴデンドロサイトに分化誘導したところ、予想どおりオリゴデンドロサイトへの分化効率が向上しただけでなく、ES細胞でさえ分化誘導が困難であった、樹状突起が発達した成熟成熟オリゴデンドロサイトにまで分化させることに成功したのである(画像5)。以上の結果から、マウス型様変換することにより、ES細胞に比べて分化能力の低いiPS細胞であっても、その分化効率を改善できることがわかったというわけだ。
より品質の高いiPS細胞を作り出す技術改良は、今後iPS細胞がさまざまな分野で有効利用されるためにも必要不可欠といえる。今回開発された技術は、マウス型化というiPS細胞自体の品質を高めることにより、分化誘導が困難な細胞へも分化させることに成功したもので、部分的にヒト型ES細胞よりも質の高いiPS細胞の樹立に至った形だ。しかし今回の研究発表では、まだiPS細胞に不安定性が残存していることも判明。今後は、マウス型"様"ではなく、真のマウス型iPS細胞への変換を目指し、さらにiPS細胞の質を高めることで不安定性を克服し、その技術をヒトのiPS細胞へ橋渡しするような研究展開が期待されるとしている。