東京大学は7月22日、塩化物イオンチャネル遺伝子「CLCN1」のスプライシングを正常化する効率のよい「アンチセンス核酸」を同定し、それを「バブルリポソーム」と超音波を用いて筋細胞に導入することで、筋強直を伴う「筋強直性ジストロフィー1型」用の新しい治療法を確立し、同方法をマウスに用いるとCLCN1のスプライシングが正常化してマウスの筋強直症状が改善したと発表した。
成果は、東大大学院 総合文化研究科 広域科学専攻の石浦章一 教授、同・古戎道典 大学院生らの研究チームによるもの。研究の詳細な内容は、7月22日付けで英オンライン総合学術誌「Scientific Reports」に掲載された。
筋強直性ジストロフィー1型は、筋肉だけでなく、全身へとさまざまな症状がおよぶ特徴がある。具体的な症状としては、筋強直や進行性の筋萎縮、心伝導障害、白内障、耐糖能異常、そして精神遅滞などだ。筋強直性ジストロフィー1型におけるさまざまな症状が生じる詳細な機構についての決定的な理解は得られていないが、いくつかの症状が遺伝子からメッセンジャーRNA(mRNA)が作られる過程の「スプライシング」という反応の異常な制御によって引き起こされることが知られている。
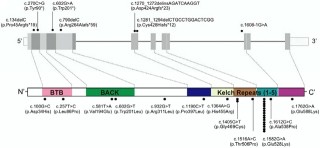
スプライシングとは、遺伝子からタンパク質が作られる過程で、DNAから転写されたmRNA前駆体の内、タンパク質に翻訳されないmRNA前駆体の領域(イントロン)を除き、タンパク質に翻訳される領域(エキソン)のみをつなげる反応のことをいう。
そして筋強直症状については、まず塩化物イオンチャネル遺伝子CLCN1に異常があることで、耐糖能異常は「インスリン受容体遺伝子」のスプライシング制御に異常がある結果として生じるということがわかってきた。塩化物イオンチャネル遺伝子とは、筋細胞膜上にあるイオンチャネルをコードする遺伝子のことで、主に塩化物イオンの透過に関わっている。このチャネルの機能が低下することで、筋肉が収縮しやすくなり、筋強直を引き起こしてしまう。またインスリン受容体遺伝子とは、細胞膜上にあるインスリンの受容体をコードする遺伝子のことで、この受容体機能が低下すると、耐糖能異常などの糖尿病様症状が出現するのである。
これらのスプライシングの異常な制御を改善することができれば、筋強直性ジストロフィー1型の症状緩和につながるため、現在までさまざまなスプライシングの改善方法が試みられてきており、「エキソン・スキップ」という方法が最良であることがわかっている。これは、アンチセンス核酸を用いて余分なエキソンの読み取りを飛ばす方法で、これにより成熟mRNAに特定のエキソンが含まれないように制御することが可能だ。実際、マウスを含む筋ジストロフィーモデル動物でも応用されている(同じ遺伝子でも、エキソンとイントロンの配置は動物種により異なる)。
アンチセンス核酸とは、DNAやRNAなど生体内の核酸と相補的な核酸配列を持ち、DNAやRNAの特定の配列に結合する人工的に設計された核酸のことである。DNAやRNAの特定の配列に結合することで、DNAやRNAの働きを阻害する仕組みを持つ。なお、アンチセンス核酸を用いてエキソン・スキップを引き起こすためには、これまで解決できていない大きな問題がある。アンチセンス核酸自体を細胞内に導入しなければならないのだが、アンチセンス核酸そのものは細胞膜を通過することができないのだ。そのため、アンチセンス核酸を効果的に筋細胞に届ける方法の開発が求められているのである。
今回の研究で石浦教授らは、まず特定の配列を持つアンチセンス核酸がマウスのCLCN1の正常型スプライシングを効率よく促進することを発見。次に、アンチセンス核酸を効率よく筋肉細胞に導入する方法として、バブルリポソームと超音波を用いた。バブルリポソームとは、脂質の膜であるリポソームに超音波造影剤である「パーフルオロプロパンガス」を封入したもので、いわば、超音波造影剤の小さな泡である(東京薬科大学の根岸洋一准教授との共同研究)。
このバブルリポソームとアンチセンス核酸の混合溶液をマウスの筋肉に注射し、筋肉に外から超音波を照射すると、バブルリポソームが筋組織内ではじけ、その衝撃で筋細胞膜に小孔が開く。この小孔により、理論的にはアンチセンス核酸を細胞内に導入できるという仕組みだ。今回の研究では、この方法を用いてアンチセンス核酸を導入することにより、筋強直性ジストロフィー1型モデルマウスのCLCN1のエキソン・スキップに成功し、筋強直症状の改善が観察されたのである。
なお前述したが、ヒトとマウスでは、同じCLCN1でもエキソン・イントロン構造に若干の違いがあるので、今後はヒトのCLCN1におけるアンチセンス核酸の効果を確認することで、筋強直性ジストロフィー1型の筋強直症状を緩和する薬剤としての応用が期待されるとしている。