基礎生物学研究所(NIBB)は7月16日、「外胚葉」、「中胚葉」、「内胚葉」の基本的な体の構造が作られる時期のマウス胚を生きたままで、従来にない高時間解像度で長時間観察することに成功し、この時期の細胞移動の様子を明らかにしたと発表した。
成果は、NIBBの市川壮彦研究員、同・野中茂紀准教授らの研究チームによるもの。研究の詳細な内容は、7月8日付けで米オンライン科学誌「PLoS ONE」に掲載された。
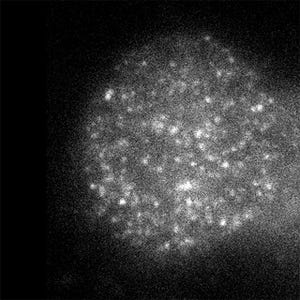
受精後6.5日(ヒトでは17日頃に相当)のマウス胚は、画像1に示されているようにお椀状の構造をしている。このお椀は、当初は2層の細胞のシートからなるが、やがて「エピブラスト」と呼ばれる内側の層にある特定の領域「原始線条」において、その一部の細胞が「臓側内胚葉」と呼ばれる外側の層との間の領域に飛び出し、さらに広がることで新しい3層目のシートの中胚葉を形成する。このダイナミックな細胞運動は「原腸陥入」と呼ばれ、その後の発生に不可欠な、発生学の教科書には必ず載っているような基本的現象だが、後述する技術的な諸問題から、ほ乳類の胚において生きた細胞運動を直接追跡することは困難だった。
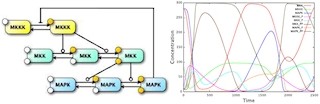
一方、欧州分子生物学研究所(EMBL)のErnst StelzerグループリーダーとPhilipp Keller博士(それぞれ現Goethe University Frankfurt、Janelia Farm研究所)らは、「ライトシート顕微鏡」と呼ばれる新しい顕微鏡法を開発。その基本原理は、画像2の通りだ。
従来の蛍光顕微鏡では、広く使われている共焦点顕微鏡も含め、XY平面の画像1枚を得るために励起光が試料全体に照射される。立体像を得るためにはZ方向の値を変えながらXY平面像を何枚も撮影し、さらに細胞の移動をとらえるためには上記を一定時間ごとに繰り返す必要がある。しかし原腸陥入の時期のマウス胚は光照射に著しく弱く、撮影のための繰り返しの光照射によって死んでしまうという問題があった。
ライトシート顕微鏡では、照射専用のレンズを用いて、シート状の励起光を側面から照射する。この方法だと、実際に観察したい部分以外には光が当たらないため、照射光の悪影響を最低限に抑えることが可能だ。かつ、この方法ではサンプルの比較的深いところまで観察できる、一般的な共焦点顕微鏡に比べて高速で撮影できるというメリットもある。
そこで、野中准教授と市川研究員らはEMBLとの共同研究を行い、ライトシート顕微鏡の1種である「デジタルスキャンライトシート型顕微鏡(DSLM)」を基礎生物学研究所に導入した。DSLMはこれまでにもゼブラフィッシュ胚などの研究に使われてきた一方、マウス胚に使用するには試料の保持方法などの問題があったのだが、新たな手法を開発することでこの問題を解決し、今回、マウス原腸陥入期胚を生きたまま丸ごと立体観察することに成功したというわけである。
さらに理化学研究所の望月敦史主任研究員、中里研一研究員との共同研究により、観察によって得られた3次元+時間の大容量データから個々の細胞を追跡するソフトウェアが開発され、エピブラストの核と中胚葉細胞の運動パターンの解析が行われた。
研究チームは、核が蛍光を発するよう標識されたマウスの原腸陥入期胚を観察した結果、2つの新たな現象を発見したのである。1つは、分厚い細胞シートをなすエピブラストの核が頂端(お椀の内側)-基底(外側)軸に添って細胞内を移動し頂端側で分裂する、いわゆるエレベーター運動がこの早い時期の胚でも起こっていることだ(画像3)。なお、NIBBのWebサイトには動画も公開されているので、興味がある方はご覧いただきたい。
核のエレベーター運動は神経上皮で見られる現象だが、その意義については未だ明らかになっていない。上皮層の分化を促すという説があるが、この時期のエピブラストではまだそのようなことは起こらないため、今回の知見がエレベーター運動の意義の解明に一石を投じる可能性があるという。
2つ目は、中胚葉細胞を1細胞レベルで追跡した結果、その運動パターンは隣接する細胞と一緒に集団として移動する「collective migration」ではなく、個々の細胞がばらばらに移動しながら、全体としては原始線条のある胚後方からも前方へ広がっていく移動様式をとることを明らかにした(画像4)。
|
|
|
|
画像3。細胞核が光る胚の輪切り画像。胚の各領域を画像1にならって色分けした。赤の矢頭は分裂中の細胞核を指す。スケールバーは20mm。A:胚の前方、P:胚の後方 |
画像4。各中胚葉細胞の追跡結果。色付けされた線が細胞の軌跡、赤い点線が原始線条の位置を表す。図中左が胚前方、図中上が胚の腹側 |
マウスはヒトと同じほ乳類であることから、医学研究において最も重要なモデル生物の1つだが、初期胚のどこにある細胞が将来どの器官になるのかといった発生パターンは、観察の技術的困難さゆえ、まだ十分に明らかになってはいない。今回の研究はこの問題を解決するブレイクスルーとなる基盤技術の1つとなるだろうという。今回開発された技術はマウス胚を使った研究に幅広く応用可能であり、それがヒトの奇形や先天性疾患の原因解明につながることが期待されるとしている。