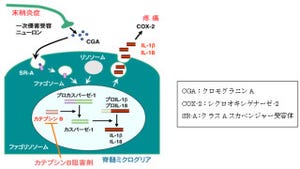
福岡大学は6月18日、九州大学、生理学研究所(NIPS)との共同研究により、糖尿病、末期がん、抗がん剤の副作用などで神経が傷害されると引き起こされる慢性的な激しい痛みの「神経障害性疼痛」の発現に、痛みの情報伝達を担うタンパク質である「ケモカイン」の1種である「CCL-1(C-C motif ligand-1)」が深く関与していることを証明することに成功したと発表した。
成果は、福岡大薬学部の高野行夫教授、本多健治助教、九大大学院 薬学研究院の野田百美 准教授、同・大学院生の秋元望氏(現・NIPS所属博士)、NIPS神経シグナル部門の井本敬二教授らの共同研究チームによるもの。研究の詳細な内容は、6月20日付けで英科学誌「Cell Death and Disease」電子版に掲載された。
神経障害性疼痛の特徴的な症状の1つが、「アロディニア」だ。これは、通常では痛みとして感じられない、例えば服が肌にこすれるといった刺激が強い痛みとして感じられるというもので、患者のQOLが損なわれてしまう。モルヒネなどの強い鎮痛薬を使用してもこの痛みを抑えることができないのが厄介で、日本はもちろんのこと、世界中で多くの患者が現在も苦しんでいるところである。
そこで研究チームは、神経障害性疼痛動物モデル(座骨神経部分結紮モデル)を作製し、CCL-1とその特異的な受容体である「CCR-8」の発現変化、脊髄内での神経細胞およびグリア細胞とサイトカイン発現に対する影響の調査を実施した(画像1)。また正常マウスにCCL-1を髄腔内に投与し、アロディニア発現が調べられたのである。さらに、CCL-1中和工対の投与もしくはCCR-8ノックダウンマウス(CCR-8を持たない)を用いて、神経損傷後アロディニア発現が調べられた。
なおCCL-1は別名「I-309」や「TCA-3(T-cell activation gene-3)」と呼ばれ、抹消において免疫細胞の「単球」および「Th2細胞」の遊走活性を示すケモカインとして知られている。またケモカインとは、白血球の遊走を引き起こす「サイトカイン」(細胞間でやり取りされる多様な生理活性を持つタンパク質の1種)の総称だ。
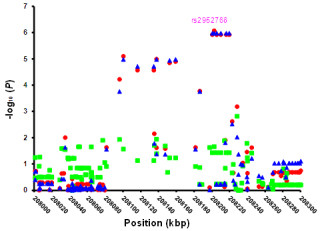
その結果、まずわかったことが、座骨神経を損傷させたマウスは脊髄後根神経節および脊髄の「CCL-1 mRNA」発現が認められ、CCR-8の発現が上昇したことだ(画像2・3)。次に、CCR-8は正常マウスの脊髄において主に神経細胞上だけでなく、「ミクログリア」および「アストロサイト」上にも存在することが確認された。
なおミクログリアとは、中枢において脳内免疫防御を司っており、ニューロンの修復を助けたり、死細胞を貪食したりする役割を持つ。またアストロサイトとは、中枢における細胞外液の恒常性の維持、血液脳関門の形成などに関与している。
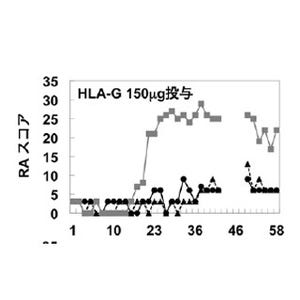
そして神経損傷前にCCL-1中和抗体を投与した結果、神経損傷によって発現されるアロディニアを有意に抑制したが、神経損傷後のCCL-1中和抗体投与ではアロディニアの発現抑制は観察されないことが確かめられた(画像4)。またCCL-1を正常なマウスの脊髄腔内に単回投与したところ、強いアロディニアの発現が発生。このCCL-1によって誘導されるアロディニアは、NMDA受容体アンタゴニスト「MK-801」によって抑制されることも判明している。
次に、CCL-1を脊髄スライス標本に作用させたところ、グルタミン酸の自発性放出の促進を示唆する「sEPSCs(spontaneous excitatory postsynaptic currents)」の頻度が上昇。続いて、CCL-1を髄腔内に投与したところ、NMDAサブユニットの「NR-1」および「NR-2B」のリン酸化が観察され、脊髄グリア細胞(ミクログリア、アストロサイト)マーカー、またサイトカインである「TNF-a」、「IL-1b」および「IL-6 mRNA」の発現が上昇することがわかった。
最後に、siRNAを用いて、CCR-8ノックダウンマウスの神経損傷により発現するアロディニアへの影響についても検討が行われ、アロディニアが抑制されることが判明したのである。
今回の成果は、モルヒネでも抑えられない神経障害性疼痛を抑えることのできる新規の薬剤開発に希望を与えるものであるという。また、将来さらなる疼痛発現メカニズムの解明の糸口となって、神経障害性疼痛の予防・治療に大変有益であることが期待されるとしている。