早稲田大学(早大)は、科学技術振興機構(JST)、東京大学、英・Cancer Research UK、かずさDNA研究所との共同研究により、「減数分裂」時に通常時よりも大幅に遠くに配置される染色体の中央部分の「動原体」を、細胞小器官の1つである「中心体」がどうやって引き寄せ、そして染色体を正しく分配して配偶子をきちんと形成しているのかという20年来の謎を、新開発のライブイメージング技術を用いて解明したと発表した。
同発表に際し、早大 先端生命医科学センター(TWins)にて、研究の責任者である早大 先進理工学部 生命医科学科 細胞骨格ロジスティクス研究部門の佐藤政充准教授(画像1)による記者会見が開かれたので、その模様をお届けする。
なお成果は、佐藤准教授、Cancer Research UKの角井康貢 氏、同・登田隆 氏、かずさDNA研究所の山本正幸所長(東大・大学院 理学系研究科・生物化学専攻教授兼任)、東大 山本正幸教授の研究室の大学院生である岡田直幸氏らの国際共同研究チームによるもの。研究の詳細な内容は、6月16日付けで英科学誌「Nature cell biology」オンライン版に掲載され、印刷版7月号にも掲載される予定だ。
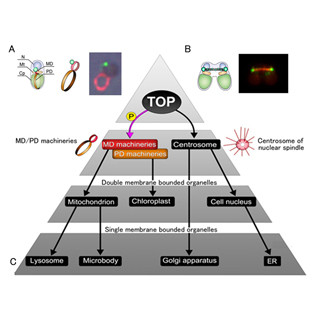
細胞分裂は、ヒトだろうが細菌だろうが生命であればみな行っていることであり、ヒトが小さな受精卵、つまり1個の細胞から60兆とも100兆ともいわれる細胞数で構成される成人の体にまで成長できるのも、この細胞分裂というシステムのおかげである。細胞分裂の流れを簡単にまとめると、まず細胞内でDNA(染色体)が複製されて2組になった後(そのほかの細胞小器官も2細胞分作られる)、1組ずつ正確に分配され、そして細胞が2つに分裂して母細胞と同じ内容の娘細胞が2つできあがるというわけだ(画像2)。
この2組のDNAを分配する際に重要な作業を担うのが、中心体とそこから生えている紡錘体である。分裂時には中心体もふたつ存在し、母細胞の両極に位置し、そこから紡錘体を伸ばしていって染色体の中央部分の動原体部分を捕まえ、左右から引っ張ることでその動原体部分から分割し(Xの字型の染色体が中央から分割されるので1本線になる)、分配が完了するというわけだ。この分裂過程のどこか1箇所にでもエラーがあると、細胞死や細胞のがん化といったトラブルが発生してしまう。
今回の佐藤准教授らの実験では、菌類子嚢菌の真核生物で単細胞である「分裂酵母」という菌が使われた。その理由は、透明なので生きたまま細胞内の挙動を観察しやすいこと、遺伝子操作が容易なこと、細胞分裂に必要な構造や遺伝子の多くがヒトなどの高等生物ともほぼ共通していること、実験室内で減数分裂を簡単に誘導できること(高等生物の減数分裂の誘導は現在の技術では極めて困難)などだ。また染色体の数がヒトだと23組あるが、分裂酵母は3組しかないので、細胞内の挙動を視認しやすいという面もある。
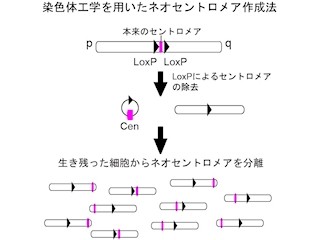
そうしたさまざまな理由で選ばれた分裂酵母は、細胞分裂の過程においてエラーを避けるためのさまざまな工夫をこらしており、その1つが動原体をあらかじめ中心体の近くに配置することで、紡錘体が動原体を確実にキャッチできるようにするというものだ(画像3)。
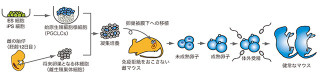
ただし、細胞分裂には特殊なケースとして、精子や卵子などの配偶子を形成するために行われる「減数分裂」がある。減数分裂があることで、染色体を混ぜて組み替えることで、同じ1人の人間でも多様なゲノム(すべての遺伝子情報)を記した配偶子を作り出せるので、同一種の中での多様性や進化といった面で重要な仕組みだ(画像4・5)。
誤解が起きやすいのでもう少し詳しく説明すると、Aさんという男性がいたとして、そのAさんが作り出す精子は、1つとして同じゲノムはない(厳密には、確率論的に事実上ゼロに近いものの、同じゲノムができる可能性はあり、一生の内でカウントすれば、生産される精子の数は膨大なので、何匹かは同じゲノムの精子を作っているかも知れない)。Aさんは、父親と母親からそれぞれからもらった遺伝子を持っているわけだが、精子を作る段階で、Aさんの父親由来の情報と母親由来の情報をシャッフルするので、ゲノムのどの部分がAさんの父親由来なのかそれとも母親由来になるのかはランダムであり(すべてがまったく異なるというわけではなく、一部は同じ、ということは当然ある)、精子のゲノム情報が1つひとつ違うというわけだ。
この配偶子形成における遺伝子の組み替えと、受精で精子と卵子由来の遺伝子が組み合わさるという部分が混同しやすいのだが、ここで話をしているのはあくまでも精子や卵子を形成する段階の話である。ともかく、このように精子も卵子も同一人物のものであっても遺伝情報の組み合わせが異なるから、同じ両親を持つ兄弟姉妹でも一卵性双生児などはまた別だが、「顔や体格などが全然似てない」などということが普通にあるのだ(両親の人種が異なれば、髪や目、肌の色が兄弟姉妹でも異なるなんてことは普通なのはご存じの通り)。
そして、この配偶子を作り出す際の遺伝子の組換えを行うには、動原体が中心体から遠く離れた場所に配置する必要があることが1994年に判明している。正確には、染色体の末端のテロメア部分が中心体にくっつき、動原体が最も遠くにある状態である(画像6・右)。
しかし、画像6・右の状態だと組み替えを行うには都合がいいが、その直後の染色体の分配は逆に行いづらいという大きな問題がある。中心体から遠く離れていては、紡錘体が動原体をつかむことができず(紡錘体の長さは0.5μmぐらい、中心体と動原体間は2μmぐらい)、染色体が2つの娘細胞に正しく分配されないリスクが高くなってしまうのだ。正しく分配されないと当然よくないわけで、正確なところはまだわかってはいないが、ダウン症候群のような異数体出生(ダウン症候群は、21番染色体が1本多い)になったり、流産になってしまったりするの原因の1つである可能性もあるという。
だとすると、実際に我々ヒトを含めて、生物は普通に子どもが生まれてくることが圧倒的に多いわけで、なぜ動原体が遠い位置にあるのに、きっちりと分配できているのかがわからなかったのである。それが今回の研究によって判明したというわけだ。
具体的には、紡錘体は微小管と呼ばれる繊維状の構造物で、いくつも中心体から生えているわけだが、減数分裂時にのみ、その内の3~4本(分裂酵母の場合であり、ヒトなどはもっと多い可能性がある)が一気に伸びて動原体にくっつき、そしてまた一気に縮むことで、動原体を中心体の近くにたぐり寄せるという仕組みがあることがわかったのである。佐藤准教授によれば、カメレオンの舌が伸びて獲物を捕らえて引き寄せるようなイメージ(ほかにも釣り竿の竿自体が伸びるイメージとも)だそうだ。
カメレオンの舌のようというと、同じ細胞間のつながり方などの構造を変化させることで伸縮しているようなイメージだが、この場合は実際にはそうではなく、紡錘体を構成する部品が次々と周囲から寄せ集まって積み上がって伸びていくのが正しい。いってみれば、レゴブロックで塔を作っていくような感じというわけだ。よって伸びるというよりも、積み上げるとか積み足すという方が正解かも知れない。
さらに、通常の分裂時には動原体には存在しないタンパク質「Alp7/TACC-Alp14/TOG(Alp7)」が、動原体に存在することも確認され、それが動原体表面にビッシリと存在していて接着剤のような働きをし、伸びてきた紡錘体を動原体にくっつける役割を果たしているということも確認された(画像7・8)。
細胞の核のサイズがおおよそ2μmで、通常時の紡錘体の長さは前述したように0.5μmほどだ。それが、撮影開始して数分後に伸び出し(画像8にはその画像は含まれていない)、4分経過時点で引っ張っている最中、4分45秒の段階ではすでに引っ張り終えているという具合で、紡錘体は数分で伸縮を終えたというわけだ。どれだけ素早い動きなのかがわかるだろうか。減数分裂全体が3~4時間かかることと比べると、なおさら素早い動きであることがわかる。
ちなみに、紡錘体がただペタっと動原体にくっついているわけではない。くっつくいた後に位置の調整がなされ、最終的に動原体側のワニ口クリップのようなものが紡錘体にガッツリとかみついてしっかりと固定する仕組みだそうだ。Alp7にくっつくのは、あくまでも動原体と接触しやすくするための仕組みで、ガッチリとロックするための仕組みは別に用意されているのである。
紡錘体が縮む時は、先端から部品がバラバラと外れて短くなっていく。かみついている部分は、部品がどんどん離れていく紡錘体の最先端よりも中心体に少し寄った位置であり、短くなると同時にかみついている位置も中心体に寄っていく(よって、かみついている位置まで分解が進んでしまって離れてしまうことは通常はない)。
例えていうなら、ファスナーのような感じといえばいいだろうか。エレメント(金属のかみ合う部分)が紡錘体で、スライダー(開け閉めする上下に動くツマミ)が動原体のイメージである。服の場合、エレメントは上側が開いているわけだが、その開いているエレメントを無理矢理さらに左右に広げると、それの強引な広げられる力で触れていなくてもスライダーが下に進んでいくが、そんなイメージと思ってもらえばいい。
ともかく、動原体は紡錘体が短くなり続けても、最先端から一定の距離を置いた中心体よりの部分にかみついたままでいるので、途中で外れたりせずに中心体のそばまで移動できるというわけである。
それから今回の解明の原動力となったのが、新開発の「生細胞3色イメージングシステム」だ。赤の「mCherry」、緑の「GFP」、青の「CFP」という3色の蛍光タンパク質を分裂酵母内に導入し、動原体を赤、微小管を緑、中心体を青に蛍光染色して3色同時に可視化するというライブイメージングシステムである。動画撮影は、秒間何コマというような一般的な感覚のフレームレートではまだ撮影できないそうで、現状では10~15秒に1枚という割合で撮影する形で、動画1は厳密にはそれらをつなぎ合わせたものというわけだ。
なお、今回の研究で「微小管が異常といえるほど長く(素早く)伸びる」ことと「Alp7が動原体に存在する」ことの2つが減数分裂の時に限って起きることがわかったわけだが、そのメカニズムまではわかっておらず、今後はそれを調べるべく分裂酵母を用いた研究を継続していくと、佐藤准教授は述べている。
またヒトやマウスなどの高等生物の減数分裂に関しては、分裂酵母のようには簡単に誘導することができなこと、観察が難しいことに加えて、紡錘体や染色体、Alp7などの挙動は未知の部分が数多く残っており、それらを確かめるためには、細胞を操作する技術や、観察技術のさらなる革新が必要だという。また、そうした高等生物における減数分裂の研究用ツールとしては、iPS細胞は利用できる可能性があるとしている(実際のところ、ヒトの場合は倫理的に難しいので、高等生命の場合は、まずはマウスになると思われる)。
さらに、不妊や流産、ダウン症候群(染色体数の異常)の原因の1つとして、紡錘体の働きが弱いため(動原体までちゃんと伸びることができない、伸びても動原体を捕まえることができないなど)、配偶子形成に異常が生じていることが原因となっているケースも考えられるという。将来的な展望としては今回の研究をより進展させて、減数分裂における紡錘体の伸縮やAlp7が動原体に存在するメカニズムを解明することで、それらの予防などに役立つことも期待されるとした。
今回の会見では、筆者としても改めて生命の神秘というか、もはやその「すごさ」を感じた。生命が地球に誕生して40億年程度とはいわれているが、それから現在に至るまでの人間の感覚では想像できない悠久の時間、全地球規模でさまざまな環境の下で気の遠くなるほど膨大な数のトライ&エラーを繰り返し続けた結果、ヒトをはじめとする生命体が誕生してきたわけだが、人類が生命のすべてを解明できる日はいつになるのだろうか? と、その奥の深さにもはや震撼してしまう。佐藤准教授も同じように生命の神秘を常に感じているそうで、今回のことも「紡錘体そのものが生き物のというか、まるで意志があるように感じましたね」と語っており、生命が持つさまざまな仕組みの凄さを改めて強調していた。