京都大学は5月29日、すい島細胞と間葉系幹細胞を融合させた細胞が糖尿病治療に有望であることを発見したと発表した。
成果は、京大 再生医科学研究所の角昭一郎准教授、同・柳井伍一研修員らの研究チームによるもの。研究の詳細な内容は、5月28日付けで米オンライン科学誌「PLoS ONE」に掲載された。
低侵襲の重症糖尿病治療法として期待される「すい島(すい臓でインスリンなどを分泌する細胞塊)」移植だが、従来の方法では移植早期に多くのすい島細胞が失われ、1人分のすい島でインスリン治療が不要になる確率は低く、また複数回の移植によってインスリン治療が不要となった場合でも、この状態を長期に維持することは容易ではなかった。
このような問題を解決するために各種の方法が検討されているが、炎症・免疫制御機能や血管新生誘導機能、アポトーシス(プログラム細胞死)制御機能などを有する「間葉系幹細胞」をすい島と共に移植することで、すい島移植の成績を向上させる試みも報告されている。
そこで研究チームは今回、ラットのすい臓からすい島を単離し、これをさらに単細胞に分散させたものと、ラットあるいはマウスの骨髄を培養して作成した間葉系幹細胞を混合し、電気的に細胞融合を行って融合細胞を作成した。融合細胞は培養20日後も「ブドウ糖反応性インスリン分泌能」を発揮したが、この時期にはすい島単独あるいはすい島細胞と間葉系幹細胞とを共培養したものではこの機能は廃絶していることが確認されたのである。
なお、ブドウ糖反応性インスリン分泌能とは、すい島細胞の非常に重要な機能であり、血糖(血中のブドウ糖濃度)が高くなるとインスリンを分泌するが、低い状態では分泌しない働きのことをいう。
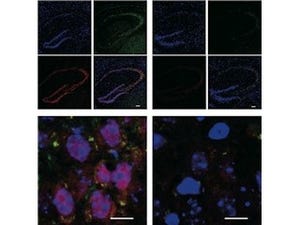
次にストレプトゾトシンの注射によって、糖尿病とした同系ラットを用いて糖尿病治療実験を実施。2000個のすい島を腎被膜下に移植すると、血糖はほぼ正常値まで低下したが、同様のすい島1000個では、すい島単独あるいはすい島と間葉系幹細胞との共移植では血糖改善効果が認められないことが判明した。一方、1000個のすい島から作成した融合細胞を移植したところ、血糖は少しずつ持続的に低下し、3カ月後には正常値には至らないものの、ほかの糖尿病ラットに比べて明らかに低い値まで低下したのである(画像)。
これを受け、ラットすい島細胞とマウス間葉系幹細胞の融合細胞を作成して遺伝子発現を検討したところ、融合細胞ではマウスのインスリンやラットの間葉系幹細胞特異的遺伝子が新たに発現していることが確かめられた。この結果は、融合細胞で間葉系幹細胞核がすい島細胞様にリプログラミングされる一方、すい島細胞の核も間葉系幹細胞様にリプログラミングされることを示しているという。このことから、融合細胞は、すい島機能を維持しつつ間葉系幹細胞の特徴も有する新たな細胞であると解釈することができるとした。
今回の成果から、研究グループは、より少量のすい島細胞を利用して、より効果的な糖尿病治療が行える可能性が見えてきたとする。具体的には、ドナー1人分の単離すい島を用いて複数人を治療できる細胞資源を作成できる可能性があり、また移植後の長期成績においても著明な改善が期待できると考えられるとしている。
さらに、再生医療推進法の成立によって、日本の再生医療環境が劇的に改善することが期待されるが、すい島細胞と間葉系幹細胞との細胞融合の臨床応用に道が拓ければ、これを作成する技術は再生医療における画期的なイノベーションの1つとなり得るのではないかと期待されるとしている。
ただし、融合細胞の細胞生物学的検討を深化させて、すい島機能維持の機構や腫瘍形成などの危険性を評価する研究が必要としており、ブタなど大型の動物でも今回と同様の検討を行った後に、将来の臨床応用に向けた研究を展開したいと考えているとしている。