九州大学(九大)は4月16日、東京大学(東大)、国立感染症研究所(NIID)との共同研究により、結核菌を認識する新しいセンサ分子(受容体)「MCL(Macrophage C-type lectin)」を発見し、さらに同センサが結核菌を最初に感知する重要な働きを担っていること、そして獲得免疫を活性化させる作用があることが明らかになったと発表した。
成果は、九大 生体防御医学研究所の山﨑晶教授、同・三宅靖延助教、同・大学院医学系学府博士課程3年の豊永憲司氏、博士課程1年の森大輝氏、東大の岩倉洋一郎教授(現・東京理科大学)、同・角田茂助教、NIID ハンセン病研究センターの星野仁彦室長らの研究チームによるもの。研究の詳細な内容は、米国東部時間4月18日付けで米国科学雑誌「Immunity」オンライン版に掲載された。
近年、日本でも「結核の再燃」や、薬の効かない「多剤耐性結核」が問題となっているが、日本はそれでもまだそれほど感染者が頻繁に出るわけではないが、世界に目をやると、70億強の人口の約3分の1が感染しているという脅威の感染症だ。
結核と人類は長い期間にわたって戦い続け、少なくとも日本では一時は「過去の感染症」となりつつあるような状況であったことから、結核のことはだいぶ理解されているものと思う方も多いことだろう。しかしそれは誤った認識で、健康なヒトの体がどのようにして結核菌を認識し、排除しているのかというメカニズムの詳細はよくわかっていないのである。
そうした中で研究チームが2009年に発見したのが、結核菌の受容体である「Mincle」という分子だ。Mincleは古くから「アジュバント」として知られていた結核菌の主成分「トレハロースジミコール酸(TDM)」を認識し、宿主の免疫応答に重要な働きを担っていた。なおアジュバントとは、投与した抗原に対する免疫応答を補助したり増強したりする物質のことをいう。
Mincleは通常ほとんど発現していないが、TDMの刺激によって白血球の1種で侵入してきた細菌などを直接食べて殺す役割を持つ「マクロファージ」や、同じく白血球の1種で侵入してきた細菌の性質を見分けて免疫の司令塔ともいうべきT細胞に伝えて「獲得免疫」を活性化させる役割を持つ「樹状細胞」で速やかに作られることがわかった。「リガンド」によって、受容体の発現が上昇するポジティブフィードバック機構と考えられる。
なお獲得免疫とは、「特異性」「記憶」を有する特徴を持った病原体を特異的に排除する高度な免疫システムで、ワクチンはこの獲得免疫を活性化させるのが目的である。またリガンドとは、特定の受容体・センサに特異的に結合する物質のことで、病原体センサのリガンドのほとんどは、病原体特有の構造を持つ。
ところがこのMincleは、感染前はほとんど発現していないため、どのようなメカニズムでMincleが作られるようになるのか、そのきっかけとなる最初の結核菌センサは不明だったのである。そこで研究チームは、Mincleに構造が比較的よく似ているMCLに注目することにした。MCLはマクロファージや樹状細胞に発現する分子として知られていたが、その認識分子や機能はまったくわかっておらず、Mincleと同様に謎の多い分子だったのである。
研究の結果、このMCLが結核菌を感知する最初のセンサであることが判明したというわけだ。また、MCLは結核菌を認識して、Mincleを速やかに発現させるという役割があることもわかった。さらに、MCLも前述したように結核菌特有の糖脂質であるTDMを認識することが明らかとなったのである。
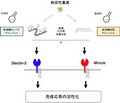
研究チームはMCLを持たないマウスを作成して結核菌で刺激したところ、Mincleが発現してこないことがわかった(画像1)。このMCL欠損マウスは結核菌に対する免疫応答が弱くなることも判明したのである。つまり、MCLは感染前から生体に準備されている新しいセンサであることがわかったというわけだ。
また、結核菌が体に入ると、最初にMCLがそれを認識して生体に知らせ、速やかにMincleを作らせていることも明らかになった(画像2)。このように、1つの病原体成分に対して恒常的センサ、誘導性センサの2つのセンサが用意されている例はこれまで報告がない。結核という強力な病原体に対抗するために、進化の過程で生物がさまざまな戦略を講じてきたことが考えられるという。
結核菌の抽出物は、古くから免疫力を上げるアジュバントとして知られていた。今回発見された新たな受容体MCLは、今後、ワクチンアジュバントのターゲット分子として、新しいインフルエンザワクチンやがんワクチンの開発に貢献することが期待されると、研究チームは語った。
また、ヒトを含む生物が結核菌に対する2つのセンサを用意していたことに対する理由として、反応を増幅してより効率のよい免疫応答を可能にする、誤作動による免疫系の暴走を防ぐ、などが挙げられるとしている。そのほかにも、MCL特有な機能があるのかも知れないという。
なお、今回の研究で、MCLはMincleよりむしろ獲得免疫を強く活性化する性質があることもわかり、研究チームはそれに対して、「興味深いこと」としている。このメカニズムはまだまったくわかっておらず、今後の課題としている。そのため、MCLを選択的に結合し、Mincleに結合しないような分子を見つけることができれば、不必要な炎症を起こさず、獲得免疫を選択的に活性化するような理想的なアジュバント(免疫賦活剤)が実現できると考えられるとしている。