東北大学は4月18日、糖尿病を対象とする細胞移植治療である「すい島」移植において、臨床現場で比較的安全とされ頻用されている免疫抑制剤「タクロリムス」が、移植後のすい島周囲における栄養血管網の新生構築を阻害することを明らかにしたと発表した。
成果は、東北大 未来科学技術共同研究センター(大学院 医学系研究科兼務)の後藤昌史教授、同・大学院 医学系研究科 先進外科の大内憲明教授、同・西村隆一医師らの研究チームによるもの。研究の詳細な内容は、米国東部時間4月17日付けで米オンライン科学誌「PLoS ONE」に掲載された。
すい島は、すい臓の中にあるホルモンを分泌する細胞の集団だ。インスリンを産生するベータ細胞を含み、健常人の場合は1つのすい臓内に約100万個のすい島が存在する。そのすい島移植などの細胞移植療法は、重症糖尿病などのさまざまな疾患に対する治療法としてすでに臨床応用が始まっているところだ。この新しい治療法は、通常全身麻酔や開腹手術を一切必要とせず、点滴の要領で短時間に終えられる点に大きなメリットがある。
そのため、従来行われてきたすい臓移植などの臓器移植療法と比べ、安全・簡便・低侵襲などの利点が着目され、次世代の中心的移植医療になると大きく期待されているが、克服すべき課題も多い。その課題の1つが移植細胞の生着率の低さだ。しかも、その原因は未だ十分に解明されていない。
研究チームによれば、細胞移植の中でも、他界した他者からもらいうける「同種細胞移植」は、自分の細胞を自分に戻す「自家細胞移植」に比べて長期的な細胞生着率が低いことが明らかとなっているという。この細胞生着率に影響を及ぼす因子はいくつか考えられており、同種細胞移植で使用される免疫抑制剤もその1つだ。
免疫抑制剤とは、他者の細胞を移植した場合、それを細菌やウイルスなどと同様に異物と見なして攻撃してしまう免疫を抑制する薬剤のことで、すい島移植においては、当初「ラパマイシン」が頻用されていた。これは血管が新たにできることを抑えてしまう血管新生抑制効果を有することが最近明らかになり、現在は、タクロリムスが標準的に使用される形に切り替わった。タクロリムスは比較的安全性が高いとされてきたが、実は移植すい島の血管新生に及ぼす影響に関してこれまでまったく検討が実施されていなかったのである。
そこで今回の研究においては、「dorsal skinfold chamberモデル」マウスと「二光子顕微鏡」を組み合わせた高感度イメージングシステムを用いて、タクロリムスが移植すい島の血管新生に及ぼす影響についての検証が行われた。また、「レーザーマイクロダイセクション」で得た移植すい島において遺伝子発現の変化の解析も行われた形だ。
dorsal skinfold chamberモデルとは、背中に観察窓を装着し、皮下の血管新生状況を経時的観察することを目的とした動物モデルのことである。また二光子顕微鏡は、組織透過性が高い近赤外線パルスレーザーを使用し、「二光子吸収過程」という特殊な現象を応用して、動物の体内深く(1mm程度)まで組織を観察することが可能な顕微鏡のことだ。そしてレーザーマイクロダイセクションは、組織切片上の極小の領域を切り出すことが可能な、顕微鏡にレーザー照射装置が接続された機器のことである。
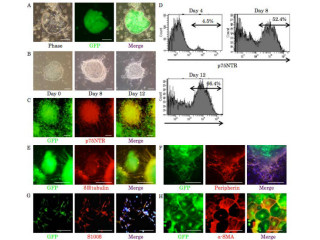
実験の結果、移植すい島に対する血管新生は移植後14日以内に完了することが明らかとなった。また、タクロリムスを投与したマウスでの移植すい島に対する新生血管体積は、投与しないマウスに比べて減少していることが判明(画像)。移植すい島の遺伝子発現に関しては、タクロリムス投与により血管誘導因子「Vegfa」の上昇が確認されたが、細胞周期への影響は確認されなかった。
画像1は、移植すい島およびすい島周囲の血管の経時的変化を撮影した蛍光顕微鏡画像。緑色蛍光タンパク質(GFP)を発現し、細胞が緑の蛍光を発するマウスから分離されたすい島を、dorsal skinfold chamberを装着したほかのマウス(レシピエント)へ移植した後、タクロリムスの効果が調べられた。移植すい島に対して新しく構築された血管を二光子顕微鏡で観察し、新生血管の体積を測定。すい島は緑、血管は赤で示されている。上段は対象群(タクロリムス投与なし)で、下段がタクロリムス投与群。
今回の研究により、タクロリムスは移植すい島からの血管誘導因子の放出制御を介さずに血管新生を抑制することが明らかとなった。従って、移植細胞の血管新生への影響を考慮した免疫抑制療法の至適化が、同種細胞移植療法の成績を改善することが示唆された形だ。
また、今回の研究において確立した高感度イメージング法と細胞の分子情報を同時に取得するシステムは、細胞移植療法のみならず、がん細胞や各種幹細胞の血管新生や生着の研究にも有用な手法となり得ると考えられると、研究チームはコメントしている。