科学技術振興機構(JST)と東京大学は4月1日、細胞とコラーゲンの混合溶液を微小な管に流しながら固めて培養することで、マイクロスケールのファイバー(ひも)形状の細胞組織を人工的に構築する方法を開発したと共同で発表した。
成果は、科学技術振興機構 戦略的創造研究推進事業ERATO「竹内バイオ融合プロジェクト」の竹内昌治リーダー(東京大学 生産技術研究所 准教授)と、プロセス融合グループの尾上弘晃グループリーダー(同・助教)らの研究グループによるもの。研究の詳細な内容は、現地時間3月31日付けで英国科学雑誌「NATURE MATERIALS」のオンライン版に掲載された。
一般的に「ひも」という形状は、絡めて太くしたり、編んでシートにしたり、2つの別の部品をつないだりと使い勝手がよい。実際、ナノスケールの機能材料(カーボンナノチューブなど)に始まって、衣服、建築物など、幅広いサイズの日常的なものづくりの材料としての基本的な形状である。
人の体内においても血管や神経、筋肉など、ひも状の生体組織が多い。そこで研究グループが取り組んだのが、ひもを使ったものづくりという考え方を組織工学に応用した、細胞組織構造体を構築するための部品(基本ユニット)としてのファイバー形状の細胞組織「細胞ファイバー」の開発だ。
今回の研究では、ファイバーの中心部(コア)をチューブ状の外殻部(シェル)が覆っている「コアシェル型」という構造を持つファイバーを「マイクロ流体デバイス」を利用して作製した。マイクロ流体デバイスとは、半導体の作製工程において利用される微細加工技術を利用して作成される、マイクロスケールの微小流路を有するデバイスの総称である。小さな空間に液体を流すため、少ないサンプル量での検査や合成など、バイオ研究や化学工学への応用研究が盛んに行われているところだ。
そしてコアには、「細胞外基質(Extracellular matrix:ECM)」の成分である「コラーゲン」や「フィブリン」に、細胞を高密度で混ぜたものが使用された。なお細胞外基質とは、生物における細胞の外に存在する超分子構造体のことだ。細胞の振る舞いを変化させることができる動的かつ機能的な物質であり、「細胞外マトリックス」とも呼ばれる。多細胞生物の場合、細胞外の空間を充填する物質であると同時に、骨格的役割や細胞接着における足場の役割、細胞増殖因子などの保持・提供する役割などを担う。
さらにシェルには「アルギン酸カルシウムゲル」という、機械的な強度が高いためファイバー形状を維持しやすく、なおかつ細胞の養分や老廃物を通過することができる材料が用いられた。アルギン酸カルシウムゲルとは、食品の添加物として工業的に利用されており、褐藻などに含まれる多糖類で食物繊維の1種である「アルギン酸」が、カルシウムイオンによって架橋されることでできるハイドロゲルだ。医療の分野では、歯科材料や手術糸などに利用されているほか、細胞のカプセル化の材料として研究用途に利用されている。
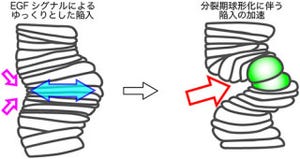
このようなコアシェル型のファイバーは培養液中で培養すると、コアで細胞が増殖して細胞ファイバーが形成される。この細胞ファイバーの形成後、アルギン酸カルシウムゲルのみを溶かして取り去ることで、細胞とECMのみで構成されたファイバー状の細胞組織が得られるという仕組みだ(画像1・2)。
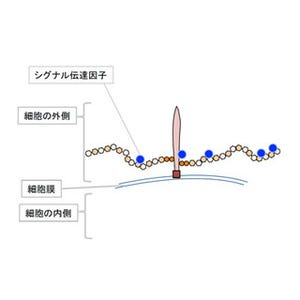
このような細胞ファイバーの作製法は非常に汎用性が高く、研究グループは神経細胞や筋肉細胞、繊維芽細胞、上皮細胞、内皮細胞を含む、さまざまな種類の初代培養細胞や細胞株で、細胞ファイバーの作製に成功した。また作製された細胞ファイバーは、各細胞の本来の機能を保持していることがさまざまな面からも確認されている。例えば、神経細胞で作製した細胞ファイバーは、ファイバー内で神経ネットワーク様の構造が構築され、神経シグナルがファイバー内を伝達することが確かめられた。
さらに血管の内皮細胞で作製した細胞ファイバーの場合は、細胞が血管様のチューブ構造を作ることが判明。筋肉の細胞で作製した細胞ファイバーは収縮運動をし、細胞ファイバー構造全体を動かしたのである。また幹細胞で作製した細胞ファイバーは、分化を誘導する化学物質によってファイバー形状のまま分化誘導が可能だった。そうした、組織の形態と機能を発現する細胞ファイバーの例が以下の画像3~6である。
|
|
|
|
画像5。ファイバー長軸方向に配向した大脳新皮質細胞ファイバー(緑:ニューロン) |
画像6。神経幹細胞からニューロンとグリア細胞に分化した神経幹細胞分化誘導ファイバー(緑:ニューロン、紫:グリア細胞、青:細胞核) |
その上、細胞ファイバーは生体に移植した場合も機能を発揮することが確認された(画像7・8)。ラットのすい臓から分離したすい島細胞で細胞ファイバーを作製し、これを糖尿病疾患モデルマウスの腎臓にカテーテルを用いて移植したところ、移植したすい島細胞のファイバーからインスリンが分泌され、糖尿病のため高血糖であったマウスの血糖値が、正常値範囲に回復することが確かめられたのである(画像9)。
そこで、同じ細胞数のすい島細胞を懸濁液のままマウスに移植することも行われたが、こちらでは血糖値を正常化できないことが確認された。細胞ファイバーの形状で移植することで、すい島細胞がより効果的に機能していることが示唆されたというわけである。研究グループによれば、今回の実験では糖尿病をモデルとして細胞ファイバーの生体内での機能を実証したが、それ以外の病気や怪我の治療などにも今後応用が期待できるという。
|
|
|
|
画像7。マイクロカテーテルによりマウス腎臓皮膜下にすい島細胞ファイバーを移植している様子 |
画像8。20cmのすい島細胞ファイバーが移植された様子。図中の矢印は、移植されたすい島細胞ファイバーを示す |
画像9は、すい島細胞ファイバーの移植による糖尿病マウスの血糖値の推移を表したグラフだ。すい島細胞ファイバーを移植後、マウスの血糖値が正常値領域に落ち着いていることが確認できる(画像の黒ドット)。また、移植15日後に移植したファイバーを除去すると、再び血糖値の上昇が確認された。また、細胞ファイバーと同じ細胞数のすい島細胞を懸濁液のままマウスに移植しても血糖値を正常化できないことから(画像の白ドット)、前述したように細胞ファイバーの形状で移植することですい島細胞がより効果的に機能していることが示唆されたというわけである。
このような細胞機能を保持した細胞ファイバーは、培養液の中でまるで日常扱う「ひも」と同様の感覚で、織ったり巻き取ったり束ねたりすることで、数センチ大の3次元組織を作ることが可能だという。研究グループでは、細胞ファイバーを織る「織機」を試作し、細胞ファイバーで布のような構造を持つ3次元組織を構築した(画像10)。
また、糸巻きのように細胞ファイバーを巻き取り、らせん状に細胞が配置された筒様の3次元組織も作製することができた(画像11)。3次元の細胞組織を「ファイバー(ひも)を利用したものづくり」というユニークな発想で作成した例はなく、将来的には血管や神経のネットワークが張り巡らされた人工組織の構築に利用可能な基盤技術となることが期待できると、研究グループは述べている。
|
|
|
|
画像10。左のイラストは細胞ファイバーを織る「織機」の模式図で、右が細胞ファイバーを織ることでできる布様の細胞組織 |
画像11。左のイラストは細胞ファイバーの巻き取りの模式図で、右が細胞ファイバーを巻き取ることでできる筒様の細胞組織 |
細胞でできたユニットを用いて3次元組織を人工的に作製する手法としては、温度応答性ポリマーを用いた細胞シートや、細胞の塊である「スフェロイド」などを用いる手法が、現在のところは一般的だ。今回の研究で開発された手法は、シートやスフェロイドなどと異なり、筋肉や神経などのファイバー状の組織を構築するのに有効なアプローチであると考えられるという。組織の機能を発現するひも状の細胞組織をメートルスケールで作製でき、それらをひもとして自在に扱う技術は世界初だという。従来の組織構築法と組み合わせることにより、より複雑で機能的な3次元組織を構築できると期待できるとも研究グループは述べている。
研究グループは今後、血管網などをこの技術によって作製し、それを用いて生体外で長期培養可能な3次元の人工組織の構築技術の確立を目指す予定だ。また移植医療への応用を目指して、iPS細胞から分化誘導された細胞を用いて3次元組織構築し、治療に役立てるための研究を展開していくことを考えているとしている。