東京大学(東大)は2月25日、神経幹細胞から産まれたニューロンが転写因子「Scratch」タンパク質を発現することによって移動を開始することを発見したと発表した。
成果は、東大 分子細胞生物学研究所の後藤由季子教授、同・伊藤靖浩助教らの研究グループによるもの。研究は、JST戦略的創造研究推進事業、チーム型研究(CREST)によって得られたもので、研究の詳細な内容は、日本時間2月25日付けで英国科学専門誌「Nature Neuroscience」に掲載された。
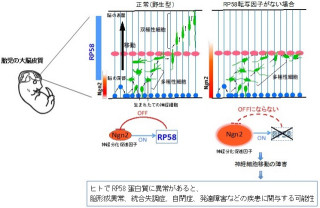
ほ乳類の脳、特に大脳では、脳の最も内側に存在し、神経系の細胞を産み出す元となる「神経幹細胞」から生み出されるさまざまな機能を持ったニューロンが順々に外側に移動する、つまり、神経幹細胞から産まれたニューロンが速やかにタイミングよく移動を開始し、適切なスピードで目的地まで移動をすることにより、そうしたさまざまなニューロンが層構造を作り配列され、それにより高度なネットワーク/計算機能を発揮することが可能となる。
これまでの研究では、ニューロンが動き始めてから目的地に到達するまでの間のニューロンの移動メカニズムの解析が中心的に行われてきたが、、神経幹細胞から産みだされたニューロンが動き始める移動の最初のステップがどのようなメカニズムで制御されているのかはわかっていなかった。
そこで今回、研究グループは胎生期のマウス大脳新皮質を用いて研究を実施。脳の深いところに存在する神経幹細胞から産まれたニューロンが、目的地である脳の表層側に向かって移動を開始するメカニズムを解明したほか、ニューロンの移動の開始において、がん悪性化などでしばしば観察される上皮間葉転換とそっくりのメカニズムが働いていることも発見したという。
具体的には、発生期のマウス大脳において、転写因子のScratchタンパク質が神経幹細胞から産生された直後のニューロンに発現していることを確認したことから、Scratchの発現を生体内で低下させたところ、神経幹細胞から産まれたニューロンが移動をうまくスタートできずに配置が異常になることが判明したという。
この結果は、神経系前駆細胞から産生されたニューロンは、Scratchの発現により移動を開始するということを示唆するものであり、これを受けて研究グループでは、Scratchがどのようなメカニズムでニューロンの移動の開始を制御するかを調査。
神経幹細胞は、発生期の大脳において神経幹細胞同士で隣り合って存在し、タンパク質「E-cadherin」を細胞の表面に発現させるが、それが隣接する細胞の表面に発現しているE-cadherinと強い相互作用を生じることで、神経幹細胞は各々の細胞の間で強固な細胞間接着を形成している。しかし調査の結果、ScratchがE-cadherinの発現を低下させることで、神経幹細胞の集団から産まれたニューロンは、周囲の神経幹細胞と接着することができなくなり、その結果、こぼれ落ちるようにして神経幹細胞の集団から離れることが示唆されたとする。
細胞同士の接着が強固な細胞集団の中から接着が弱い細胞が産まれ、集団からこぼれ落ちる現象はがん細胞の悪性化でも見られる「上皮間葉転換」として知られており、今回の研究結果はニューロンの移動の開始が上皮間葉転換にそっくりのメカニズムで制御されていることを示唆するものであるが、上皮間葉転換はがん細胞の悪性化に関わるだけでなく、個体の発生に重要な種々の場面で用いられる現象ながら、これまで脳の発生に関わるという証拠は得られていないことから、脳の発生に上皮間葉転換が関わっていることを示唆する初めての成果になることが考えられると研究グループは説明する。
なお研究グループは今回の成果から、精神疾患の原因の1つと考えられているニューロンの移動や配置の異常の解明や治療方法の開発に繋がる可能性が期待できるとコメントしている。