東京大学(東大)は、高分子ミセル型ドラッグデリバリシステム(DDS)を開発し、メッセンジャーRNA(mRNA)の中枢神経系への安全な送達・機能発現に成功したと発表した。
成果は、東大大学院 工学系研究科 マテリアル工学専攻/同・大学院 医学系研究科 疾患生命工学センター 臨床医工学部門の片岡一則教授、東大大学院 医学系研究科 疾患生命工学センター 臨床医工学部門の位髙啓史 特任准教授らの研究グループによるもの。研究の詳細な内容は、日本時間2月14日付けで米オンライン科学誌「PLoS ONE」に掲載された。
脳や脊髄などの中枢神経系疾患は、神経細胞が障害を起こすと、その機能回復が難しいことから根治的治療が困難な難治疾患の代表例だ。mRNAはタンパクやペプチドなどの生理活性因子を産生させる機能を持つため、新たな核酸医薬としての活用が期待されている。
しかし、mRNAは不安定で生体内では急速に分解されてしまうほか、自然免疫機構を刺激して、生体内で強い炎症反応を引き起こすことから、これまで治療への応用例はほとんどなかった。
今回の研究では、mRNAを内包させたナノ粒子である高分子ミセルを脳脊髄組織のくも膜下腔へ投与したところ、脳から腰髄にかけての広い範囲で、mRNAからの効率のよいタンパク発現が得られたほか、投与後5日間にわたって脳脊髄液への発現タンパクの分泌が確認されたという。
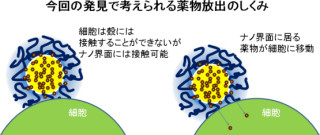
通常、細胞内でのmRNAからのタンパク発現は数時間から長くても1日程度で消失してしまうほか、体内へmRNAをそのままの形で投与したとしても、強い炎症を引き起こすのみで、タンパク発現はほとんど観察されない。しかし、今回のシステムを用いた場合、mRNAが高分子ミセル内に安定に保持されるため、エンドソームに存在する自然免疫機構による認識を回避しつつmRNAを細胞質へ送達することが可能となるほか、細胞質内でmRNAが徐々に放出されるため、長期持続的なタンパク発現が可能となったものと研究グループは説明する。
なお、研究グループは、同システムを活用することで、アルツハイマー病などの根治的治療法のない脳神経疾患や完全な機能回復が難しい脊髄損傷などの神経外傷に対して、mRNAを用いた新たな治療法の開発・早期実用化に繋がることが期待されるとコメントしている。