東京都医学総合研究所(東京都医学研)は、脳の形成を決める遺伝子を制御するタンパク質として、マウス胎児脳の実験により、神経細胞(ニューロン)が脳を作り上げるための移動過程で、ヒトにもある転写因子「RP58(Repressor Protein 58kDa)」が神経分化促進遺伝子「Ngn2」を適切なタイミングでスイッチをオフにしていること(遺伝子発現のスイッチ機能)を発見したと発表した。
成果は、東京都医学研の丸山千秋主席研究員、同・岡戸晴生副参事研究員らの研究グループによるもの。研究の詳細な内容は、米国東部時間2月7日付けで米国科学雑誌「Cell Reports」オンライン版に掲載された。
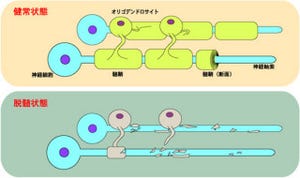
胎児における大脳皮質の形成時、神経細胞は脳深部の「脳室帯」で発生し、その後、脳表に向かって移動を行い特定の位置に定着することが知られている。もし、この移動がうまくいかないと大脳皮質の層構造が乱れ、神経回路形成の障害となってしまうが、この過程に関わる遺伝子の突然変異についての詳しいメカニズムはこれまでわかっていなかった。
遺伝子はスイッチである転写因子により、オン/オフの調節を受けるが、今回研究グループは、マウスの脳ができる際、新生ニューロンが脳表面に向かってスムーズに移動するために、「RP58」が神経分化促進遺伝子である「Ngn2」遺伝子を適切なタイミングでオフにする「抑制スイッチ」としての機能を持つことを明らかにした。
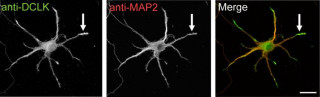
具体的には、RP58遺伝子が欠失した「RP58ノックアウトマウス」を用いて、脳の新生ニューロンが移動する状況についての詳細な研究を実施したところ、ノックアウトマウスは正常な野生型マウスと比べてニューロンの移動障害が見られ、その要因を詳しく調べたところ、RP58がない脳では、Ngn2の発現が異常に亢進していることを確認したという。また、この異常発現を実験的に抑制したところ、移動障害がレスキューされるなどの結果が得られ、この結果、ニューロンの移動過程でスムーズに脳表に向かって移動するためには、RP58がNgn2の発現を抑制する必要があることが判明したという。
ちなみにNgn2自体もスイッチタンパク質の1つで、RP58遺伝子をはじめ複数の標的遺伝子の転写をオンにすることでニューロン分化が進んでいくことが知られており、今回の知見と併せると、RP58タンパク質は、自らの遺伝子をオンにしたスイッチ遺伝子を、今度はオフにするという負のフィードバック制御機構を担うことが示される結果となり、遺伝子発現のオンとオフのタイミングが大脳皮質の層構造の構築に重要であることが示されることとなった。
なお、ニューロンの移動障害は脳形成異常や統合失調症、自閉症などの精神・神経疾患および発達障害を引き起こすことから、RP58のヒトでの解析により、これら疾患の病因解明や新しい治療法の開発につながることが期待されると研究グループはコメントしているほか、将来的に脳の再生医療の際、神経細胞が正しく配置するための手法開発の基盤となることも期待できるともコメントしている。