精神・神経医療研究センター(NCNP)は、脳と腎臓内で硫化水素(H2S)を効率よく生成する第4の経路を新たに発見したと発表した。
成果は、NCNP 神経研究所 神経薬理研究部の木村英雄部長、同・薬物動態研究室の渋谷典広室長らの共同研究グループによるもの。研究の詳細な内容は、1月22日付けで英国オンライン科学誌「Nature Communications」に掲載された。
H2Sといえば、温泉地などでお馴染みの卵の腐敗臭を持つ毒ガスとしての印象が強い。しかし、木村部長らは、そんな毒ガスのイメージがあるH2Sが、脳では神経伝達調節因子として機能していることを1996年に世界で初めて報告し、翌1997年にはH2Sが血管弛緩を誘導することを明らかにした。
さらに、2004年にはH2Sが神経細胞を酸化ストレスから保護する機能も発表。この発見は、心筋や腎臓を「虚血再灌流障害」から保護する働きの発見へとつながっている。
H2Sによる細胞保護機能はほ乳類にとどまらず、細菌が示す抗生物質抵抗性もH2Sによって調節されていることが明らかとなり、今日では生物種を超えたユニバーサルな防御機構であると認識されるに至っている状況だ。H2Sのこうした特性を応用した新たな抗生物質開発も期待される。
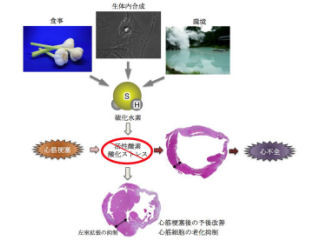
生体内においてH2Sは、システインから生産される。通常、生体内のアミノ酸は「セリン」や「アスパラギン酸」などの一部を除き、L型異性体のみが存在している具合だ。木村部長らは2009年までに3つの生産経路を報告しており、その3経路もすべてL型異性体の「L‐システイン」を基質として合成するものである。
しかし、今回発見された第4の経路は「D‐システイン」を基質として合成することが大きな特徴だ。L‐システインを基質とする経路に比べ80倍効率よく生合成することも判明している。
これまでは、L‐システインを基質とするH2S生産酵素が探索されてきたが(画像1)、今回発見されたH2S生産経路は、D‐システインを基質とする経路として初めてのものだ。
第4のH2S産生経路では、「D‐アミノ酸酸化酵素(DAO)」によりD‐システインから「3-メルカプトピルビン酸(MP)」が合成され、これが「3-メルカプトピルビン酸硫黄転移酵素(3MST)」によって代謝されてH2Sが産生される(画像1)。
L‐システインを基質とする産生経路は多くの組織に存在するが、DAOと3MSTは小脳と腎臓のみに局在するため、D‐システインを基質とするH2Sは小脳と腎臓で多く合成される仕組みだ。
一般にL‐システインは興奮毒性を示すため、大量に投与することは危険である。しかし、D‐システインは毒性が低いため、より安全なH2Sの供給源として投与が可能だ。今回の研究では、マウスへのD‐システインの経口投与により、腎臓の虚血再還流障害を顕著に軽減することも証明された。
H2Sは細胞保護因子・神経伝達調節因子として脳腎臓間をはじめとした脳臓器間ネットワークにより、臓器恒常性維持に関わっていると考えられる。今回明らかになったD‐システインから生合成されたH2Sは、現在国家的課題となっている腎疾患対策に光をあてるものだ。
腎疾患患者数は年々増加しており、腎不全による死亡は日本国民の死因の第8位(平成23年度)を占めている。これら慢性腎不全の原因の43%が糖尿病性腎症によるものだ。
腎機能障害は生命を脅かす危険性があるため、重症化した場合には透析療法を導入することが少なくない。しかし、一度導入すると長期間の透析を強いられ、透析患者のQOLを向上することが大きな課題となっている。
このような腎不全の原因となる腎臓虚血再還流障害には、フリーラジカルや活性酸素による生体膜脂質の過酸化障害が関与すると考えられている。これまでの研究で、H2Sには酸化ストレスで低下した細胞内の「グルタチオン(GSH)」の生産を上昇させ抗酸化作用を回復させることを明らかにしてきた。
また、H2Sのインスリン分泌調整機能、「膵島ベータ細胞」の保護作用も報告済みだ。L‐システインよりも効果的にH2Sを生成し、副作用の少ないD‐システインあるいはその誘導体が、慢性および急性腎障害、糖尿病性腎症の予防や重篤化を防止する治療薬、移植腎臓の保護薬として適用されることが期待されると(画像2)、研究グループはコメントしている。