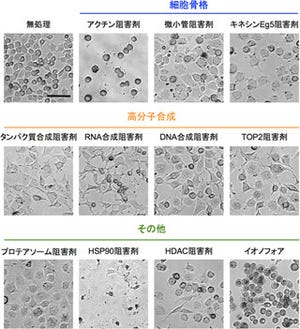
理化学研究所(理研)は12月21日、土壌に棲む「糸状菌」の仲間が、新しい抗がん剤の種となる化合物として注目される「テルペンドールE」を生合成するメカニズムを明らかにしたと発表した。
同成果は、理研基幹研究所 長田抗生物質研究室の長田裕之 主任研究員、本山高幸 専任研究員らによるもので、詳細は米国の科学雑誌「Chemistry and Biology」に掲載された。
糸状菌は、主に土壌中に存在し、二次代謝産物を生産する微生物として知られている。抗生物質として有名なペニシリンや、血中コレステロール低下薬剤のスタチンなどの有用物質を生産する能力を持つため、医薬や農薬の種となる化合物の主要な供給源の1つとなっているが、その有用物質を得るために糸状菌を単離して試験管内で純粋に培養すると、有用物質を生産しなくなる現象が頻発することから、安定に生産する手法の開発が求められていた。また、糸状菌は、肝細胞がんの原因物質のアフラトキシンや食中毒の原因の1つであるトリコテセンなどのかび毒も生産するため、かび毒を制御する手法の開発も課題になっている。
研究チームは2003年に、埼玉県秩父市の土壌から単離した糸状菌(Chaunopycnis alba RK99-F33)が生産する「テルペンドールE」が、抗がん剤の標的分子の1つであるキネシンEg5を阻害することを見いだしている。キネシンEg5の阻害は、他の標的分子を阻害することに比べ副作用が少ないため、テルペンドールEは、副作用が少ない新しい抗がん剤の種となる物質として注目されるようになってきたが、糸状菌によるテルペンドールEの生産が安定しないため化合物の大量生産が困難で、かつ構造が複雑で人工的な有機合成も難しく、創薬研究はなかなか進んでいなかったのが現状である。
また併せて、Chaunopycnis alba RK99-F33は、類似の構造のかび毒「テルペンドールC」も生産するため、その生産制御が求められていた。テルペンドールCは、家畜に重大な被害を及ぼす強力なかび毒で牧草の汚染を引き起こす「ロリトレムB」と構造が似ているため、テルペンドールCの生合成メカニズムを明らかにすることができれば、構造が類似したさまざまなかび毒の生産制御が可能になるとも期待されていた。
今回、研究チームでは、そうしたテルペンドールEの生合成メカニズムの解明を目指した研究を進めた。まず、テルペンドールE生産菌を純粋に培養して経時的に生産される化合物を分析したところ、テルペンドールEがごく一時的に生産され、すぐに消失し、その後、テルペンドールCが生産されることを見いだした。この結果から、純粋に培養したテルペンドールE生産菌は生産能を失っておらず、テルペンドールEはテルペンドールCの生合成中間体であるとの予想が立てられた。
|
|
|
テルペンドールE生産菌のコロニー。およそ2週間純粋培養したテルペンドールE生産菌。菌の名前「Chaunopycnis alba RK99-F33」のalbaは「白い」を意味しており、白いコロニーを形成する特徴がある |
この仮説を証明するために、テルペンドールEとテルペンドールCの生合成に関与する遺伝子を単離して解析したところ、テルペンドールEと構造が似たかび毒のパキシリン、アフラトレム、ロリトレムBの既知である生合成遺伝子情報を参考に、 テルペンドールE生産菌から7個の生合成遺伝子(terP、terQ、terK、terM、terB、terC、terF)の単離に成功し、これらの7遺伝子のうち、terPを破壊するとテルペンドールEが大量に蓄積するようになることが確認されたことから、terPの遺伝子産物がテルペンドールEの変換に関与していることが明らかとなった。また、同時にかび毒のテルペンドールCが蓄積しなくなったため、テルペンドールEはテルペンドールCの生合成に重要であることも判明した。
次に、terPの遺伝子産物の詳細な反応を明らかにするため、terP以外の6個の生合成遺伝子をすべて取り除いた変異株を純粋培養し、培養液にテルペンドールEを滴下。その結果、テルペンドールEは新規化合物(13-デスオキシテルペンドールI)に変換されたほか、terQ以外の6個の生合成遺伝子をすべて取り除いた株を純粋に培養し、培養液に13-デスオキシテルペンドールIを滴下したところ、13-デスオキシテルペンドールIはさらに別の化合物(テルペンドールCの生合成中間体)に変換されることが確認された。
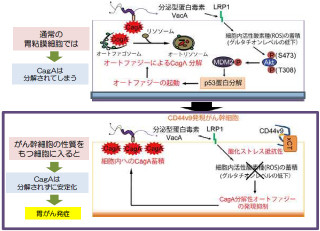
さらに、テルペンドールEの生合成経路を明らかにするために、terQ以外の6個の生合成遺伝子をすべて取り除いた株を純粋培養し、培養液に3個のかび毒に共通する生合成中間体パスパリンを滴下。その結果、パスパリンがテルペンドールEに変換されることが確認され、このことから、テルペンドールEはパスパリンから酵素TerQの働きで合成されることが明らかとなり、これらの結果から、テルペンドールEがテルペンドールCの生合成におけるカギとなる中間体であることが明らかとなり、生合成中間体は一時的生産物であるために、テルペンドールEの生産が不安定になることが判明した。
なお研究チームは今後、同定した7個の生合成遺伝子を操作することで、テルペンドールEより効果が高い化合物を、安定的に大量に生産できる可能性があるとするほか、ロリトレムBは、テルペンドールCと構造が似ていることから、ロリトレムB生産菌も生合成中間体としてテルペンドールEを生産している可能性があるとのことで、ロリトレムBなどのかび毒の生産制御も可能になることが期待されるとしている。