京都大学は12月5日、ヒトのミトコンドリアで「ニコチンアミドアデニンジヌクレオチドリン酸(NADP)」を合成する酵素を特定し、NADPの供給源を明らかにしたと発表した。
成果は、京大 農学研究科の村田幸作教授、同・河井重幸助教らの研究グループによるもの。研究の詳細な内容は、12月4日付けで英国科学誌「Nature Communications」オンライン版にオープンアクセス誌として掲載された。
ヒトを含めた真核細胞は、分裂し、増殖する「オルガネラ:ミトコンドリア(Mt)」を持っている。ヒト細胞のMtは、外膜と内膜に囲まれ、内膜は複雑な「クリステ構造」を取る(画像1)。Mtは独自のDNA(mtDNA)を数コピー持ち、分裂し、増殖する点が特徴だ。
Mtは細胞質に数1000個存在しており、Mtは糖や脂肪酸を燃焼させ、エネルギー(ATP:アデノシン三リン酸)を産生する重要な機能を担う。したがって、Mt内では多種多様な酸化還元反応が稼働しているが、その酵素反応に必要な補酵素(NADPと「ニコチンアミドアデニンジヌクレオチド(NAD)」)の中、NADPの供給源が不明なため、Mt機能の解析の妨げになっていた。
NADPは、酵素NADキナーゼが触媒する反応の「NAD+ATP→NADP+アデノシン二リン酸(ADP)」で合成される。しかしヒト細胞では、細胞質に1個のNADキナーゼ(ヒトNADキナーゼ)の存在が知られているのみで、NADキナーゼの遺伝子も1個しかないとされてきた(画像2)。これでは、Mtにおける「NADP(H)」(NADPHは還元型NADPの略)供給源がなく、Mtの機能を説明することができない。
しかしヒトと同じ真核生物である植物では細胞質、葉緑体、「ぺルオキシソーム」に、酵母では細胞質とMtにNADキナーゼが存在し、その反応によってNADPが供給される(画像2)。Mtの機能を考えた場合、ヒト細胞のMtにNADキナーゼが存在しないということは想定し難いというわけだ。
そこで、ヒト細胞のNADキナーゼを詳細に調査。その結果、タンパク質「C5orf33」がMtのNADキナーゼと特定された次第だ。実際、C5orf33はMt輸送配列を持ち、Mt局在性も免疫学的手法で証明された。つまり、C5orf33は細胞質で合成された後、Mtに輸送されるという仕組みを持つ(画像3)。
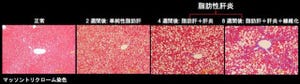
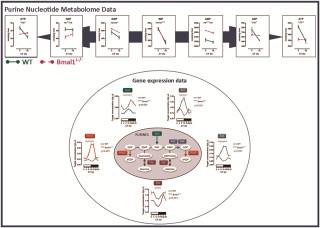
また、C5orf33はMt内の生理的条件下で機能し、ほぼすべての臓器での発現が確認された(画像4)。さらにC5orf33は、ATPに加えて「ポリリン酸(リン酸重合体)」に高い活性を示す原核細胞型の酵素であり、ヒトMtが原核細胞由来であることを示唆した。こうした成果により、ヒトMtの機能と起源を理解する学術的に重要な成果が得られたのである。
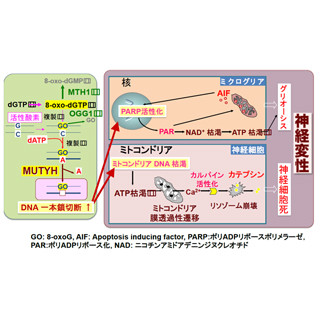
Mtの機能低下(特に、Mtで発生する活性酸素やそれに起因したATP生産能の低下)は、アルツハイマー病、パーキンソン病、老化、糖尿病、動脈硬化、心不全、がんなど、多くの疾病「ミトコンドリア病」を引き起こす。NADP(H)は、エネルギー生産反応や活性酸素消去反応にも関与しており、かかる疾病に対する新たな予防・治療法の開発が期待されるという。