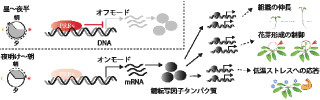
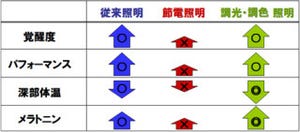
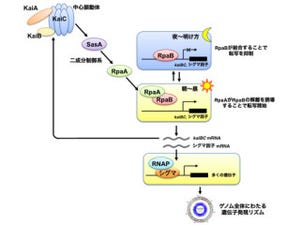
理化学研究所(理研)は10月17日、「サーカディアンリズム(概日時計)」と呼ばれる24時間周期のリズムと、睡眠・覚醒に伴う神経活動(睡眠・覚醒機能)が、神経伝達物質「セロトニン」の働きによって脳の深部で統合され、24時間周期の睡眠・覚醒リズムが形成されることを見出したと発表した。
成果は、理研 脳科学総合研究センター シナプス分子機構研究チームの宮本浩行客員研究員(科学技術振興機構さきがけ研究者)、同・発生神経生物研究チームの濱田耕造研究員、米ペンシルベニア大学の中丸映子博士、米ハーバード大学のヘンシュ貴雄教授らの国際共同研究グループによるもの。
今回の研究成果は、JST戦略的創造研究推進事業 個人型研究(さきがけ)研究領域「脳神経回路の形成と制御」における研究課題「脳回路網の再編成における睡眠の役割」の一環として行われ、研究の詳細な内容は、米科学雑誌「The Journal of Neuroscience」の10月17日号に掲載された。
単細胞生物から植物、動物、ヒトに至るまで、生物はサーカディアンリズムを自律的に示している。このサーカディアンリズムは精神活動、体温、ホルモン分泌、神経活動、タンパク質・遺伝子発現など、あらゆる生物現象に認められ、とくにヒトや動物の活動基盤をなす睡眠・覚醒も強いサーカディアンリズムの制御を受けている。
これまでに、脳深部の小さな神経核である「視交叉上核(SCN)」がサーカディアンリズムの主時計であることが確認されており、分子生物学的知見も数多く報告されてきた。
しかし、SCNからの信号がどこに伝えられ、睡眠・覚醒のサーカディアンリズムがどう形成されるのかというシステムに関する基本的な理解は進んでいない状況だ。
SCNは小さな神経核のため、行動する個体からその神経活動を記録するのは容易ではない。また、出力先が広く多岐にわたっていること、睡眠・覚醒制御に関与する脳領域が分散し、それらの相互作用が未解明であることなども研究を困難にしているのである。
そこで研究グループはこれまでに、うつ病や情動、摂食、睡眠などとの関連を指摘されてきたセロトニンを数時間で選択的に除去する物質を開発し、ラットの睡眠・覚醒のサーカディアンリズムがセロトニンの働きを必要としていることを報告した。
今回、その手法を利用し、睡眠・覚醒リズムが崩壊した脳の各領域の神経活動パターンを数週間にわたって調べ、サーカディアンリズムと睡眠を結ぶ神経メカニズムの解明に取り組んだのである。
研究グループは、自由に行動しているラットの睡眠・覚醒を記録すると共に、脳の各領域の脳波を測定して、神経活動を数週間にわたって記録した。具体的には、狙った脳部位に細い金属線を埋め、そこでの神経細胞群が興奮する時に生じる電気信号を検出して、神経細胞の活動状態が調べられた。
その結果、従来の知見どおり、SCNや「前脳基底部・視索前野(BF/POA)」(画像1)をはじめ、脳の多くの領域で神経活動レベルが24時間周期で上昇・下降するサーカディアンリズムが観察され(画像2)、睡眠・覚醒機能についても、睡眠時は神経細胞の活動が低下し、覚醒時は活性化することが確認された。
|
|
|
|
ラットのSCNとBF/POAの位置と神経活動の様子。画像1(左):ラット脳断面図で視交叉上核(SCN:赤)、前脳基底部・視索前野(BF/POA:青)は脳の底部に存在している。画像2:SCN、BF/POAをはじめに脳の多くの領域で、神経活動が24時間周期で振動するサーカディアンリズム(この場合、正確には光の影響下にある日周リズム)を観察した |
|
次に、研究グループが開発された物質をラットに投与して、脳内のセロトニンを除去した。この物質は、セロトニン合成のもととなるアミノ酸の1種「トリプトファン」を選択的に分解する酵素「tryptophan side chain oxidase I(TSOI)」で、脳内のセロトニンを数時間以内で5分の1程度に急速、選択的かつ可逆的に減少させることができる。
ヒトより短い時間の睡眠・覚醒サイクルを持つラットにこの物質を投与すると、昼夜を通してさらに短い周期で睡眠と覚醒を繰り返すようになり、睡眠量や行動量のサーカディアンリズムが崩壊した(画像3中、下)。
しかしこの時のSCN の活動は、通常通り強固なサーカディアンリズムを維持すると共に(画像3上)、正常な睡眠・覚醒機能(睡眠時の神経活動低下と覚醒時の活性化)を確認できた。この傾向は、大脳皮質などほかの脳領域でも同じだった。
画像3は、セロトニン除去によるサーカディアンリズム、睡眠・行動量の変化。SCNが生み出すサーカディアンリズムは、セロトニン除去物質投与後(TSOI)でも、通常通り強固な24時間神経活動のリズムを維持した(上)。一方、睡眠・行動量を見ると、物質投与により24時間周期は崩れた(中、下)。
しかし、睡眠・覚醒を直接的に実行する前脳基底部・視索前野(BF/POA)の神経活動に着目すると、サーカディアンリズムが顕著に減少していることが判明したのである(画像4)。
そこで、セロトニン受容体機能を阻害する薬物「リタンセリン」を、正常なマウスのBF/POA領域に局所的に投与したところ、睡眠の大部分を占める徐波睡眠のサーカディアンリズムが阻害された(画像5)。
|
|
|
|
BF/POAが生み出すサーカディアンリズムと睡眠のリズム。画像4(左):睡眠・覚醒を直接的に実行する領域のBF/POAでの24時間神経活動リズムが、セロトニン除去物質投与後(TSOI)、顕著に減少した。画像5:セロトニン受容体機能を阻害する薬物リタンセリンをBF/POA領域に局所投与すると、徐波睡眠の24時間リズムが選択的に阻害された。一方、レム睡眠のリズムは影響されなかった |
|
これらにより、セロトニンの働きを受けたBF/POA領域は、SCNが生み出すサーカディアンリズムを受け取って睡眠・覚醒機能と時間的に統合し「睡眠・覚醒のサーカディアンリズム」を作り出すと結論した(画像6)。
画像6は、SCNとBF/POAによる睡眠のサーカディアンリズム。セロトニン系の働きによって活性化したBF/POAの領域が、SCNからのサーカディアンリズムを受け取って睡眠・覚醒機能と時間的に統合する。その結果、「睡眠のサーカディアンリズム」を作り出す。
脳の多くの領域における神経細胞の活動は、サーカディアンリズムと睡眠・覚醒機能の両者の制御を二重に受けていると考えられる。
脳や身体の健康を保つには、各領域間の協調と共に、秒、分、時間、日の単位で刻々と必要となる機能を時間的に協調させることも重要だ。今回の成果は、サーカディアンリズムと睡眠・覚醒が、神経活動として脳の各領域で時間的にどう結び付けられているのか、その一端を解明したものとなったほか、セロトニン神経系が、不眠、睡眠リズム障害、うつ病や統合失調症などの精神疾患と複雑に関連することが示唆された。また、今回注目された前脳基底部は、アルツハイマー病との関わりも指摘されており、高齢化社会に伴う諸問題も睡眠やサーカディアンリズムと切り離すことはできないという。
そのため今回の研究をさらに進めることで、現代社会において看過できないこれらの疾患の新しい治療法につながると期待していると、研究グループは述べている。
また研究グループは今後、サーカディアンリズムと睡眠の統合機構メカニズムを神経回路レベルで調べると共に、12時間あるいは48時間周期リズムを持つ動物や、脳の左右でリズム位相の異なる動物の機能設計を通して、例えば視覚情報処理やシナプス可塑性・記憶といった脳機能とリズムの詳細な解明を目指すとしている。