慶應義塾大学(慶応大)は8月29日、心筋梗塞モデルマウスの心臓に3つの「心筋誘導遺伝子」を導入し、梗塞巣の「心臓線維芽細胞」を直接心筋細胞に転換することに成功したと発表した。
成果は、同大医学部の家田真樹特任講師、稲川浩平助教、福田恵一教授らの研究グループによるもの。また今回の研究は、JST戦略的創造研究推進事業 チーム型研究(CREST)の一環として行われた。研究の詳細な内容は、日本時間8月日29付けで米国科学雑誌「Circulation Research」オンライン版に掲載された。
心筋梗塞などの心臓病では心筋細胞が失われるが、ヒトを含む哺乳類は失われた心筋細胞を元に戻す自己再生能力を持っていない。梗塞部位など心筋が消失した部分は、心臓内にある線維芽細胞が増殖し線維化により置き換えられるが、この細胞は拍動できないため心臓ポンプ機能が低下する。
そのため、従来の心臓再生の方法としては、ES細胞やiPS細胞のように成体を形成するすべての細胞へと分化できる幹細胞をまず培養皿上で作製し、次に心筋細胞を誘導し、患部へと移植する方法が期待されているところだ。
しかし、ES細胞やiPS細胞などの幹細胞を用いた心臓病への細胞移植治療の課題として、幹細胞の心筋細胞への分化誘導効率が低いこと、分化誘導後に得られる細胞の中に目的外の細胞や未分化な細胞が残存している可能性、このような細胞群を体内に移植した場合のがん化の危険性などがある。ES細胞に関しては、倫理的な問題もあるところだ。さらに、拍動している心臓へ移植後の細胞の長期生着は困難であり、臨床応用にはまだいくつかのハードルがあるという。
こうした問題点は、患者の心筋梗塞部位の心臓線維芽細胞を、幹細胞を経ず直接心筋細胞に転換できれば回避できる可能性がある。心筋細胞の細胞数は心臓を構成する細胞の内では全体の30%程度。残りの70%近くはポンプ機能を持たない心臓線維芽細胞で占められている。
また心筋梗塞、心不全などの病気では心筋細胞が減少し、この心臓線維芽細胞がさらに増殖し、線維化、心不全を悪化させてしまう。心臓内に多数存在するこうした線維芽細胞を心筋細胞へと直接転換することができれば、幹細胞使用による前述の問題点を回避できる可能性があるというわけだ。
そう考えた家田特任講師らは、心筋細胞を直接誘導できる「心筋誘導遺伝子」(iPS細胞を樹立するときの「山中ファクター」にあたる)として、3つの遺伝子「Gata4」、「Mef2c」、「Tbx5」を2010年に同定することに成功していた。
そして、この3つの心筋誘導遺伝子を培養皿上のマウスの線維芽細胞に同時に導入することで、iPS細胞を経ることなく心筋細胞を直接作製することに成功した(画像1)。しかし、生体内に直接心筋誘導遺伝子を導入するだけで、心筋梗塞部位の線維芽細胞を心筋細胞へ転換できるかどうかは不明だった。
今回の研究で稲川助教、家田特任講師らはマウスを用い、心臓に心筋誘導遺伝子を導入して、心臓線維芽細胞から直接心筋細胞を作製できるかどうかを検討した。
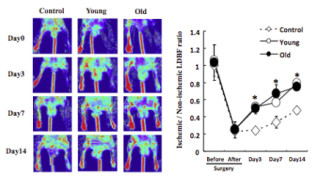
方法として、まず心臓の栄養血管である冠動脈を結紮(けっさつ:糸で冠動脈を結び血流を遮断)し、マウス心筋梗塞モデルを作製。冠動脈結紮当日(心筋梗塞発症日)に、開胸下で注射器を用いレトロウイルスベクターにより遺伝子導入を実行。最初に陰性対照のウイルス液を導入したところ、線維芽細胞から心筋細胞の誘導は見られなかった。
次に、3つの心筋誘導遺伝子のウイルス液をそれぞれ100倍に濃縮し組み合わせて、計30μlを心筋梗塞患部に直接注射。その結果、梗塞部の線維芽細胞の内、1週後に約3%の細胞が心筋遺伝子に誘導され、2週後に1%の細胞で心筋タンパク質の発現が見られた。心筋の成熟を表す横紋構造は、心筋タンパク質を発現した細胞の15%に見られた。
今回の研究過程で、同様の方法で心筋誘導因子を用いて生体内で心筋細胞を直接作製できたという結果が、2012年4月と5月に相次いで欧米2つの研究グループから報告されている。
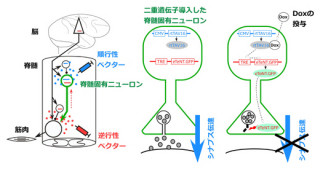
そこで家田特任講師らは、さらに新生心筋細胞の成熟度を改善するため、3つの遺伝子を同時に導入できる「ポリシストロニックウイルスベクター」(画像2)を開発。このウイルス液30μlをマウス心筋梗塞患部に注射したところ、心筋タンパク質を発現した新生心筋細胞の内の30%で横紋構造を確認することに成功し、3つの遺伝子を別々のウイルスベクターで導入した場合と比較し成熟心筋の誘導効率を2倍に改善することに成功した。
今回の研究結果より、Gata4、Mef2c、Tbx5という3つの遺伝子を効率よく導入することで、生体内でも心筋梗塞部位の線維芽細胞から心筋細胞を直接作製できることが判明。
生体内で心筋を直接再生するという今回の技術はこれまでにない新しい心臓再生法であり、他臓器の再生でも応用できる可能性がある。以上より今回の研究結果は臨床上、再生医療実現化の端緒となる重要な知見を示すものと考えるという。
また、今回の技術は従来の線維芽細胞からiPS細胞を作製し、それから心筋を誘導し、さらに心筋を分離精製したのち患部に移植するというこれまでの心臓再生の工程を短縮単純化したため、幹細胞使用に関わる特有の問題点も解決することが期待されるという。
なお、遺伝子導入や心筋誘導効率の改善、ヒトでの安全性など課題もあるが、今回の研究結果は心臓再生医療実現を前進させる大きな一歩であると考えられると、研究グループはコメントしている(画像3)。