北海道大学(北大)は、強力な免疫活性細胞として知られる樹状細胞ががん組織内において、「TIM-3」というタンパク発現を新たに獲得することを明らかにした。同成果は、同大遺伝子病制御研究所附属感染癌研究センターの地主将久氏のほか、同大院医学研究科腫瘍内科学および病態医科学、順天堂大学医学研究科免疫学、香川大学医学部免疫病理学、アイオワ大学内科学との共同研究によるもので、「Nature Immunology」に掲載された。
抗がん剤による治療への耐性発現は、がん患者の生命予後を決定する重要な要因となるため、抗がん剤耐性獲得に至るメカニズム解明が、がん根治を目指した治療法の開発に重要となる。
抗がん剤耐性の成因は、主にがん細胞自体の遺伝子変異に起因するとされているが、近年になり、がん細胞周囲に存在する血管細胞や免疫細胞の役割も報告されるようになってきた。しかし、その詳細な分子メカニズムについてはほぼ解明されていないのが現状であり、そのため、抗がん剤への応答性を調節する免疫制御因子を同定しその作用機序を解明することが求められていた。
今回の研究グループでは、免疫活性を司る代表格である樹状細胞を対象として、がん組織に存在する樹状細胞の機能のうち、がん細胞から発せられる「警報」(センサ)を感知する免疫システム(自然免疫)の活性の変化に注目して研究を行った。
特に、がん特異的に樹状細胞による自然免疫活性制御を司る因子の同定と、その因子が抗がん剤応答性に与える影響について検証を行った結果、通常はがん細胞の排除に働くと考えられていた免疫活性細胞である樹状細胞が、がん組織中では自然免疫活性の抑制に関与することを発見した。また、その免疫抑制に重要な役割を果たすのが、がん組織に存在する樹状細胞に特異的に高発現している「TIM-3」という分子であることを同定した。
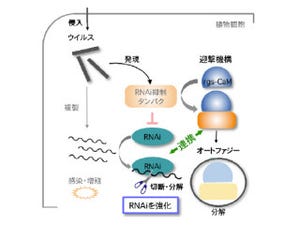
主に抗がん剤刺激によりがん細胞より放出されるDNAは、自然免疫活性センサとして働いているが、その活性には「HMGB1」というタンパクとDNAとの結合が重要であることは以前から知られていたが、今回の研究により、TIM-3はHMGB1と競合的に結合することで、DNAによる有効な自然免疫活性を抑制する働きを有することが明らかとなった。
また、TIM-3阻害剤ががん細胞由来のDNAに対する自然免疫活性能を回復することで、抗がん剤による大腸がん拒絶能が劇的に改善することも見出し、これらの結果から、本来はがん拒絶にはたらく樹状細胞が、TIM-3を介することで、逆に抗がん剤の効果を抑制するという機能転換の仕組みが明らかとなった。
研究グループでは、今回の成果を受けて、がん組織中の樹状細胞に特異的に発現し、抗がん免疫活性の抑制に関与する分子の同定をさらに推し進め、その役割を検証することで、樹状細胞発現分子を標的とする新たなタイプの抗がん剤の開発が可能になると考えられるとコメントしており、これは既存の抗がん剤への感受性を高め、再発や転移など発がんの進行を抑止するうえで、有力な武器になりうると考えられるとしている。