東京大学は7月19日、産業技術総合研究所(産総研)の協力を得て、X線結晶構造解析と核磁気共鳴(NMR)法を駆使して、胃がん発祥の危険率を優位に高めるとされるピロリ菌(ヘリコバクター・ピロリ)が産生する「CagAタンパク質」の立体構造の解明に成功したと発表した。
成果は、東大大学院 医学系研究科 病因・病理学専攻 微生物学分野の畠山昌則教授、産総研 バイオメディシナル情報研究センターの千田俊哉主任研究員らの研究グループによるもの。研究の詳細な内容は、7月19日付けで米国科学誌「Cell Host & Microbe」に掲載された。
胃がんは全世界部位別がん死亡の世界第2位を占め、毎年約70万人がこの悪性腫瘍で命を落としていると累計されている。中でも日本は胃がんの最多発国として知られ、毎年5万人が胃がんで死亡している状況だ。
近年の研究から、ピロリ菌の胃内持続感染が胃がんの発症に必須の役割を担うことが明らかになってきた。中でも、CagAと呼ばれるタンパク質を産生するピロリ菌の感染は胃がん発症に深く関わることから、胃がん発症におけるピロリ菌CagAの役割に大きな注目が集められている。
CagAは、約1200個のアミノ酸が連なって作り出される大きなタンパク質(分子量約13万)で、そのカルボキシ末端側領域には、「グルタミン酸(E)」-「プロリン(P)」-「イソロイシン(I)」-「チロシン(Y)」-「アラニン(A)」の5つのアミノ酸からなる「EPIYAモチーフ」ならびに16のアミノ酸からなる繰り返しモチーフの「CMモチーフ」と呼ばれる特徴的な繰り返し配列が存在している(画像1)。
画像1は、ピロリ菌CagAタンパク質の模式図。EPIYAモチーフが繰り返し存在しており、CMモチーフと共に、CagA尾部に集中して存在する特徴的な配列となっている。
これらのモチーフは、SHP2やPAR1を含むCagAの主要な細胞内標的分子群との相互作用を直接媒介する配列である。CagAはその全長を通してほかの既知のタンパク質とアミノ酸配列の相同性がまったく見られないことから、ほかのタンパク質の統計情報からCagAの立体構造をコンピューター予測することは不可能であった。
CagAはピロリ菌の体内で産生された後、菌が保有する「IV型分泌機構」と呼ばれるミクロの注射針を介して胃の細胞内に注入される。胃細胞の細胞膜には「ホスファチジルセリン(PS)」というリン脂質が存在しており、細胞内に侵入したCagAはPSと結合することで細胞膜の内面に付着する仕組みだ。
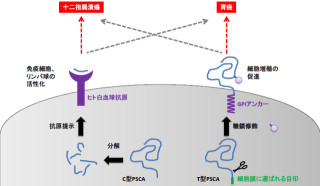
細胞膜に付着したCagAは、CMモチーフを介して胃の上皮機能維持に必須の役割を担う「セリン/スレオニンキナーゼPAR1」と結合し、PAR1の働きを抑制することで細胞が敷石状に並んで構築する胃粘膜の構造を破壊するのである(画像2)。
CagAはまた、EPIYAモチーフ中のチロシン残基がリン酸化修飾を受けることにより、SHP2と結合する能力を獲得する。CagAとの結合によりSHP2は異常に活性化され、細胞をがん化するための異常な分裂・増殖シグナルを生成する(画像2)。
画像2は、上で説明したとおりの、ピロリ菌CagAによる細胞内シグナルの撹乱の模式図だ。胃上皮細胞に感染したCagA陽性ピロリ菌は、IV型分泌機構を介してCagAタンパク質を宿主細胞に注入。細胞内に侵入したCagAは細胞膜内面に分布するホスファチジルセリンとの結合を介して膜局在に局在する。
その後、PAR1と結合することによってPAR1のキナーゼ活性を抑制する形だ(画像左側への矢印の流れ)。一方、同時にCagAはチロシンリン酸化修飾を受けた後、ヒトがんタンパク質として知られる「チロシンホスファターゼSHP2」と結合することによりSHP2を異常活性化する(画像右側への矢印の流れ)。
これらの細胞内標的分子との相互作用により、CagAは上皮細胞構造の破壊と異常な細胞増殖シグナルを誘引し細胞をがん化へと向かわせるというわけだ。
このように、ピロリ菌CagAは胃の細胞内に侵入した後、種々の宿主細胞側分子と相互作用し、それらの分子機能を障害することで胃の細胞をがん化させると考えられている。しかしながら、CagAが胃の細胞内で多種多様な分子と相互作用し発がん活性を発揮する分子構造基盤はこれまでまったく不明だった。
研究グループは今回、ピロリ菌CagAが「がんタンパク質」として働くための分子構造基盤を明らかにするため、X線結晶構造解析法ならびにNMR法を駆使してCagAの立体構造を明らかにした。
この研究成果で、EPIYAモチーフやCMもチーフを含むCagA分子の後半部分(分子全体の30%のことで、以降はCagA尾部と呼ぶ)は、固有の高次構造を持たない「天然変性構造」であることがわかった(画像3)。
画像3は、CagAタンパク質の立体構造の模式図。CagA体部(全体の約70%)を精製・結晶化し、X線結晶構造解析により結晶構造を決定したところ、3つのドメイン(ドメインI~III)からなる新規の折り畳み構造を形成していた。
画像はαヘリックスをらせんリボン状で、βストランドを平板矢印状で示している。CagA尾部も同様に結晶化を試みたがタンパク質結晶は得られず、NMR解析の結果、この領域は一定の高次構造を形成しない天然変性構造であることが見出された。天然変性構造の画像は複数の構造を行き来する平衡状態にある様子を模式的に示されている。
天然変性構造は、さまざまなほかのタンパク質に合わせて自己の形状を自在に変化させながら結合する構造として近年注目を浴びているタンパク質の形状だ。特に、高等真核生物が持つタンパク質で多く見つかっている。
この天然変性構造を用いて、CagAはPAR1やSHP2そのほか多くの標的分子との相互作用を可能にしていることが判明した。一方、CagA分子の前半部分(分子全体の70%のことで、以降CagA体部と呼ぶ)は3つの構造ドメインからなり、既知のタンパク質構造とは類似性を見ないN字型の固いコアを持つ新規の立体構造を有していた(画像3)。
また、CagAとPSの結合には、CagA分子の中央部に多数集中して存在する塩基性アミノ酸の「パッチ」が重要であることがわかった。CagAの細胞膜への付着はこの塩基性パッチと酸性のPSとの間で形成されるマジックテープ様の結合様式によると考えられた(画像4)。
画像4は、塩基性パッチとPSの結合を介したCagAの細胞膜局在の模式図。CagAの結晶構造から、体部ドメインIIの表面に正電荷をもつ塩基性アミノ酸が集中して存在した「塩基性パッチ」を構成していることが判明した。
細胞膜成分のPSは負電荷に帯電しているため、塩基性パッチとPS間の相互作用によりCagAが細胞膜局在している可能性を検証するため、塩基性パッチを構成するアミノ酸を無電荷アミノ酸に置換したところ、CagAの細胞膜局在が失われたのが確認されたのである。この結果から、マジックテープのようにCagA表面とPSが結合するモデルが強く示唆された。
加えて、PAR1やSHP2と直接結合するCagA尾部は塩基性パッチと反対側に存在するため、この細胞膜結合様式によりCagAが複数の標的分子と複合体を形成するために適した配向になることが推察されたのである。
同研究グループはさらに、可動性に富むCagA尾部の一部が固い構造を持つCagA体部の表面に付着することで、投げ縄(ラリアート)状のループが作り出されることが見出された(画像5)。
このループ形成の結果、CagAと標的分子間の複合体形成がさらに安定化し、より強いがん化シグナルが生成されることがわかった(画像5)。このことから、CagAの体部と尾部間の相互作用は発がん活性を増強させる分子内スイッチとして働くと結論づけられた。
画像5は、立体構造に依存したCagAの機能制御機構の模式図。CagAは、高次構造を形成したCagA体部(ドメインI-III)と天然変性構造のCagA尾部(点線)から構成される。
CagAの標的分子であるPAR1やSHP2はCagA尾部に直接結合する。このCagA-PAR1またはCagA-SHP2複合体の形成効率は、CagA体部のドメインIIIとCagA尾部との間の相互作用によって制御されることが明らかになった。
すなわち、CagAは分子内相互作用を形成することでPAR1やSHP2と効率良く複合体を形成するようになり、より強くこれらの標的分子の機能を脱制御する能力を獲得する。その結果、異常ながん化シグナルが増幅されることが明らかになった。
今回の研究は、ピロリ菌病原因子CagAの3次元分子構造を世界に先駆けて解明したものであり、CagAが胃細胞内標的分子を脱制御し細胞秩序を撹乱する分子構造基盤ならびにその活性制御機構を明らかにした。
この成果はCagAによる発がんメカニズムの理解を大きく前進させるものであり、胃がんの発症機構を大きく前進させると共に、世界中で多くの命を奪う胃がん撲滅に向けた分子標的治療・予防法開発への道を拓くものとして期待される。